如果有一种"时光胶囊",能让70岁的老人身体机能倒退回50岁,不仅活得更久,还能在晚年保持活力、远离疾病,你会愿意尝试吗?虽然这听起来像科幻情节,但科学家们已将它变为现实。
4月15日,一项由美国赛诺根公司(Seragon)联合清华大学和国药赛诺根的科学家共同完成的研究,在《Drug Design, Development and Therapy》(《药物设计、开发与治疗》)期刊上正式发表。他们开发了一种口服复合药物SRN-901,在相当于人类70岁的老年小鼠身上实现了中位寿命延长33%的突破,同时让衰老带来的身体机能衰退减缓了七成,肿瘤发生率风险也下降了30%[1]。

这份数据不仅是数字的突破,更意味着衰老干预研究正从针对单一靶点的“精准打击”,转向协调多通路的“系统重塑”。
SRN-901将寿命延长33%,效果超越经典药物
该研究在设计上体现了高度的科学性,实验直接选用相当于人类老年阶段的18月龄小鼠(相当于人类50多岁),这不仅验证了SRN-901的预防潜力,更证明了其在衰老已发生时的治疗价值,临床应用前景更为明确。
先来看结果。赛诺根的数据不负众望,在相同条件下,单独使用NMN或NR对小鼠寿命并无显著改善。而SRN-901将小鼠的中位剩余寿命从263.5天延长至350.5天,增幅达33%。这一效果甚至超过了以延长寿命著称的雷帕霉素,这印证了单一路径干预的局限性的同时,凸显了多靶点协同作用的优势。
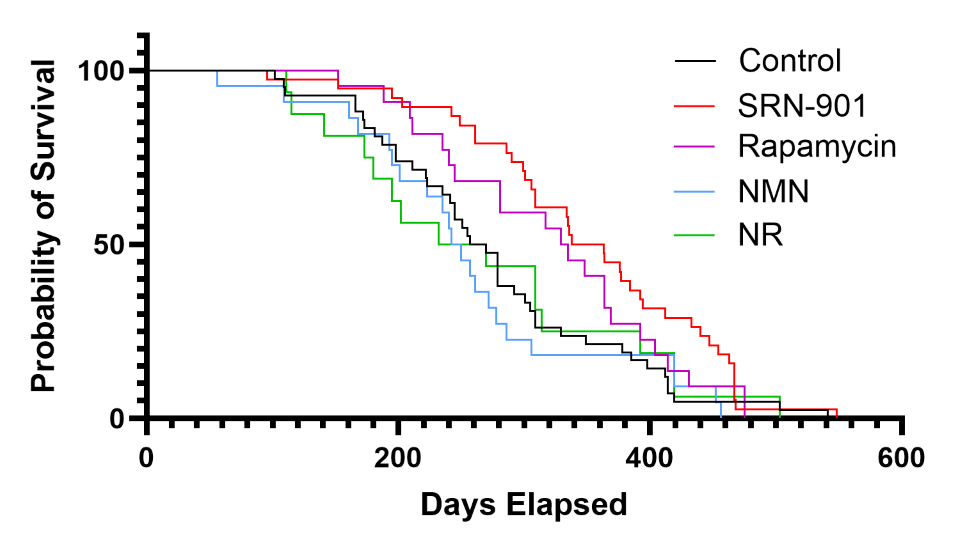
SRN-901改善健康寿命——不仅活得更久,也活得更健康
除了中位寿命的绝对延长,SRN-901还实现了显著的健康寿命改善。
从外观上看,对照组小鼠随着衰老逐渐出现毛发变白、脱落和脊柱后凸等问题。SRN-901治疗使小鼠衰弱进展减缓70%,没有出现上述问题,皮肤状态也从“苍白松垮” 变得“紧致粉嫩”。
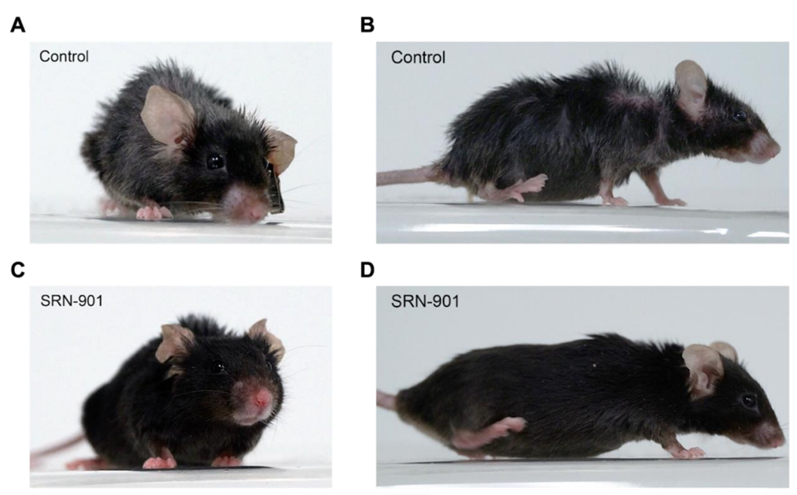
此外,SRN-901治疗还降低了小鼠的衰弱评分和肿瘤发生率,显著提升了健康寿命,减少了衰老相关疾病风险。
研究人员通过观察小鼠身体的8个方面(皮肤、体型、肌肉骨骼、眼睛、鼻子、消化、泌尿生殖和呼吸系统),根据小鼠不同部分的衰弱程度给予评分(0、0.5、1分),结果发现,与安慰剂相比,SRN-901将小鼠的衰弱进展减弱了70%。小鼠的尸检报告也显示,SRN-901将肿瘤发生率降低了30%。
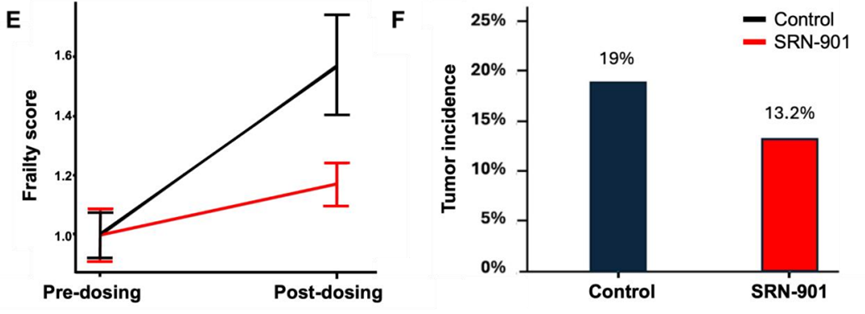
SRN-901在成年小鼠中抑制衰老相关疾病通路,同时激活与长寿相关的转录通路
研究没有停留在宏观数据上,赛诺根的科学家们接着对了SRN-901的延寿机制进行了深度挖掘。他们利用转录组学、代谢组学和蛋白质组学这三大现代生物技术,给细胞做了一次全面的“CT扫描”,揭示了SRN-901如何从分子层面系统性逆转衰老。
1. 基因层面(转录组学):下调“衰老程序”,上调“修复程序”
血液RNA的分析发现,SRN-901 治疗的小鼠中与 DNA 修复相关的通路上调,而与炎症反应、活性氧通路和 mTORC1 信号传导相关的通路均下调。
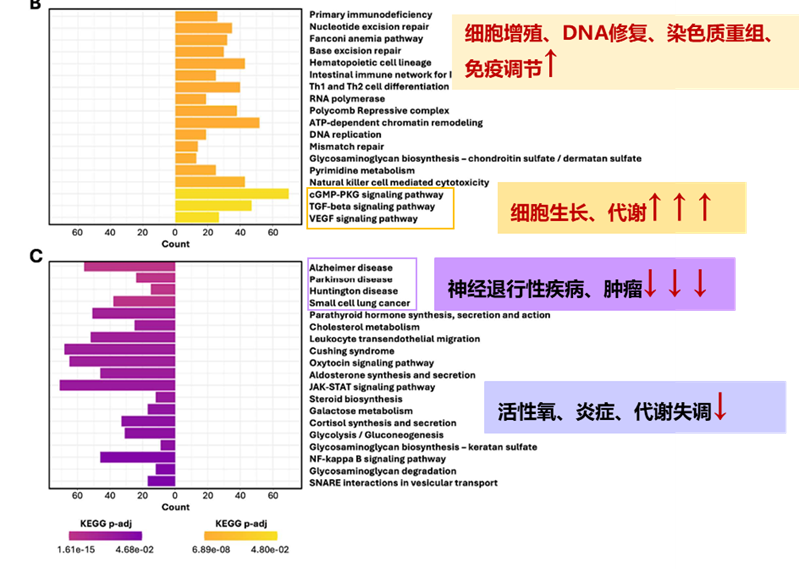
2. 代谢层面:逆转代谢年龄,重塑“年轻代谢谱”
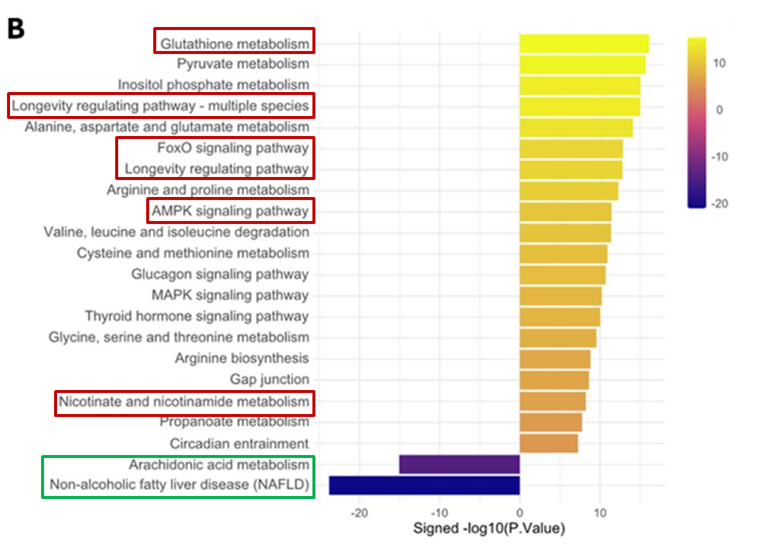
代谢是衰老最敏感的维度之一。研究者通过分析小鼠的用药前后的全血代谢物发现,有78种代谢物,在SRN-901治疗下被减弱、甚至逆转回年轻状态。其中SRN-901上调的通路有谷胱甘肽代谢、胰岛素信号、AMPK信号、FoxO信号等经典长寿通路;下调的则包括促炎性的11β-前列腺素E2、与脂质代谢紊乱和细胞凋亡相关的神经酰胺CerP等炎症和代谢失调相关通路的代谢物。
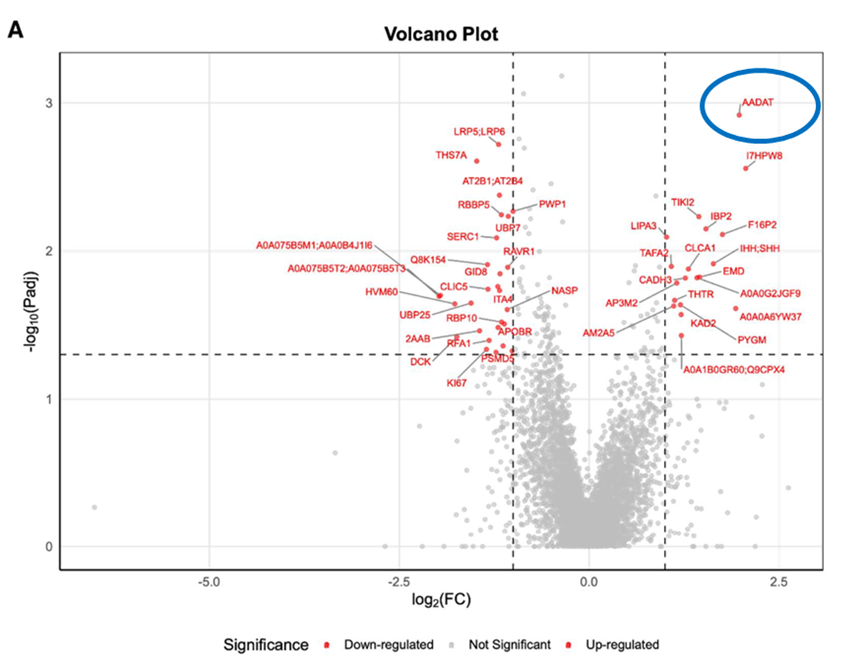
3. 蛋白层面(蛋白质组学):发现关键枢纽蛋白AADAT
研究者在超过1万个被检测的蛋白质中,发现犬尿氨酸/α-氨基己二酸转氨酶(AADAT) 是上调最显著的蛋白。AADAT参与色氨酸和α-氨基己二酸的代谢,并参与几种氨基酸和神经递质相关通路,表明与代谢和神经调节过程的潜在联系。
因此,SRN-901通过上调AADAT,可能系统性地减轻脑部的炎症与兴奋性毒性,保护神经功能,这为其在干预阿尔茨海默病、帕金森病等神经退行性疾病方面的潜力提供了关键机制线索。
SRN-901赢在哪?
SRN-901能有如此亮眼的效果,最重要的原因在于研究团队参透了衰老的本质是由多通路调控的,早早布局了多靶点干预衰老的研究。
那么,为什么单一靶点走不远?
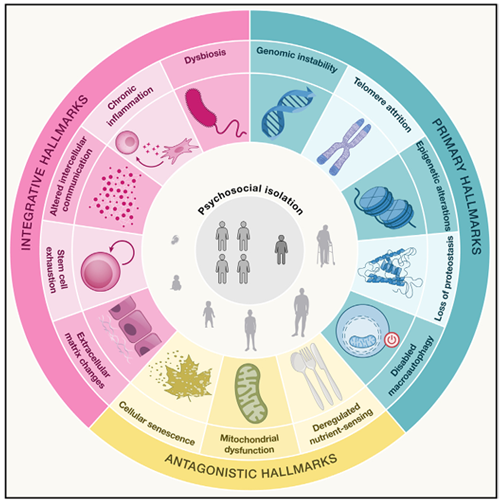
衰老并非由单一基因或通路控制,而是一个涉及基因组不稳定、慢性炎症、代谢失调、细胞自噬功能下降等多达十余项生理变化的复杂网络过程。
过去几十年,科学家们尝试过多种单一靶点策略,例如抑制mTOR通路(如雷帕霉素),或提升NAD+水平(如NMN/NR)。这些方法虽能在一定程度上延长实验动物的寿命,但效果有限,且常伴随副作用,或仅在生命早期干预时有效。
SRN-901的设计,正是直面这种复杂性。 SRN-901并非单一成分,而是由多种活性物质组成的“鸡尾酒疗法”。其思路借鉴了对抗癌症等复杂疾病的经验:通过多成分协同,同时调节衰老网络的多个关键节点,旨在实现“1+1>2”的协同效应,更系统、更稳健地延缓甚至逆转衰老进程。
为什么说SRN-901是标杆之作?
综合来看,SRN-901树立了抗衰老药物的三重标杆:在生命后期干预仍有效,打破了需从年轻时开始的局限;通过多通路协同实现了比单一药物(如雷帕霉素)更强的效果和更好的安全性(研究中未观察到体重下降等毒性);利用控释技术优化了多种成分的协同递送,这解释了为何简单混合难以复制其效果。
当然,这项研究也有待完善之处:目前仅在C57BL/6J单一品系中验证,未来需在遗传背景更多样的小鼠及人类中重复。尽管如此,这项研究依然具有里程碑意义——它首次在哺乳动物中系统验证了多靶点组合疗法对抗衰老的可行性。
SRN-901的意义远超一款候选药物。它证明了一件事:面对衰老这张复杂网络,"多管齐下"确实优于"单兵突进"。未来的"长寿药"很可能不再是某个"神奇分子",而是一套能够智能调节多层面稳态的"系统方案"。
全球老龄化浪潮汹涌,延长健康寿命已成为最紧迫的社会议题之一。SRN-901及其代表的研究方向,正在推开一扇通往更长寿、更健康未来的大门。人类战胜衰老的梦想,或许将迎来真正的转折点。
"让长寿触手可及"——赛诺根的这句口号,听起来不再像遥远的承诺。
参考资料:
[1] Weiss, B. et al. SRN-901, a novel longevity drug, extends lifespan and healthspan by targeting multiple aging pathways. www.dovepress.com (2026) doi:10.2147/DDDT.S594895.
[2] Whitehead, J. C. et al. A Clinical frailty Index in aging mice: Comparisons with frailty index data in humans. The Journals of Gerontology Series A 69, 621–632 (2013).
[3] Kroemer, G. et al. From geroscience to precision geromedicine: Understanding and managing aging. Cell 188, 2043–2062 (2025).
