从1961年海弗里克首次在体外观察到细胞衰老之后[1],科学界逐渐发现了人类衰老的原因之一——衰老细胞,并慢慢搞清楚了它们对人体产生的不利影响。长寿之家Changshou.com在《我们为什么会衰老?我们可以对抗衰老吗?》中曾经详细介绍过这段故事。
当细胞老去时,衰老细胞会产生衰老相关分泌表型(SASP,就是与衰老相关的一系列细胞因子),导致身体出现慢性炎症并诱导周围正常细胞衰老,同时加速免疫细胞衰老,降低免疫功能,使其无法清除衰老细胞和炎症因子,形成炎症与衰老的恶性循环[2],最后导致组织变性、关节炎症和与年龄相关的肿瘤等问题。
为了降低它们带来的影响,衰老干预的一个重要途径就是通过希诺裂(Senolytics,衰老细胞清除剂),这个概念最早由梅奥医学中心的詹姆斯·柯克兰(James Kirkland)提出,近年来不少新研究都是基于这个思路进行。
利用免疫系统清除衰老细胞的新手段
今年12月初,浙江大学医学院附属第二医院/转化医学研究院的研究团队在《自然·衰老》期刊上提出了一种全新的、安全且可持续的清除衰老细胞的方法[3]。他们设计了一种小分子多肽,给免疫细胞和衰老细胞做起了“媒人”,促进免疫细胞识别并清理衰老细胞,从而缓解衰老相关的病理特征,并抵抗自然衰老。
这个新方法是基于“谷氨酸能够增强免疫细胞活性”以及“衰老细胞表面有特异性受体”的原理,将谷氨酸和能结合衰老细胞特异性受体的物质组装到一起,形成一种嵌合肽E16-uPA24,起到为免疫细胞和衰老细胞“牵线搭桥”的作用。
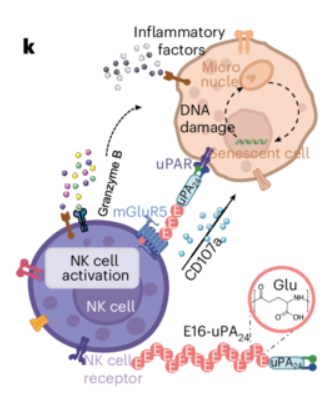
简单解释就是,衰老个体的免疫细胞活力太低了,低到已经无法识别衰老细胞并破坏它。而研究人员发现免疫细胞之一的自然杀伤(NK)细胞表面有谷氨酸受体,能与谷氨酸结合,结合后的NK细胞就像喝了咖啡一样振奋。
同时,研究人员又知道所有衰老细胞的表面都有一种独特的标志物,方便与其他细胞区别开来。研究人员一琢磨,如果能专门让衰老细胞端着“咖啡”,那NK细胞闻着味不就来了。
因此,嵌合肽E16-uPA24应运而生,一端可以结合衰老细胞,另一端可以连接自然杀伤(NK)细胞,由它从中间“斡旋”,促进NK细胞和衰老细胞的识别与结合,从而帮助杀死并清除衰老细胞。
随后,科研人员就利用衰老小鼠进行了验证,证实了这一嵌合肽可以改善慢性肝纤维化、急性肺纤维化等衰老相关疾病,并可以有效抵抗自然衰老。
D+Q:希诺裂先行者
在利用免疫细胞清除衰老细胞这个思路之前,开头提到的希诺裂之父柯克兰使用的是一种叫“D+Q”的办法。
其中,D指的是达沙替尼(Dasatinib,一种酪氨酸激酶抑制剂,常用于治疗某些类型的白血病和其他癌症),Q是槲皮素(Quercetin,简称Q,一种黄酮醇化合物,有抗氧化和抑制炎症反应的作用),D+Q作为最初被开发出来的衰老细胞清除剂,近年来取得了不少进展[4]。

大量研究表明,口服D+Q可缓解小鼠疾病模型中的多种疾病[5-7]。比如,间歇性口服D+Q可增强24月龄小鼠(相当于人类约80岁)的心脏和血管功能,改善心脏射血功能,减少血管钙化;还可以降低心脏中衰老细胞的堆积,部分逆转与年龄相关的心肌肥大和左心室纤维化等。
在针对遗传性肥胖小鼠的实验中,D+Q可增强其胰岛素敏感性,并减少与肝脂肪变性相关的衰老细胞积聚,同时还能改善肥胖小鼠的神经炎症,减轻焦虑。
此外,D+Q对治疗小鼠与年龄相关的肌肉减少症、认知功能障碍、骨质疏松、神经功能障碍、虚弱、早衰等疾病、保护血脑屏障以及延长健康寿命都有一定的益处。
D+Q的神奇之处还在于,它拥有字面意义上的“逆龄”效果。意大利麦格纳格拉西亚大学的研究人员在体外诱导培养具有衰老表型的人类心脏器官,随后用D+Q治疗。结果显示,衰老心脏出现了逆转,不仅SASP分泌的少了,心脏的活力和功能也得到了一定恢复,甚至补充了心脏前体细胞(一种在心脏发育过程中起关键作用的细胞类型,具有分化成心肌细胞、心内膜细胞和心外膜细胞等成熟细胞的能力),同时恢复了与年龄相关的再生缺陷[8]。
此外,《自然·医学》期刊上的一项临床实验显示,对绝经后女性进行间歇性衰老干预(D+Q)治疗后发现,在衰老细胞负荷较高的参与者中,骨形成增加了34%,骨吸收减少11%。也就是说,在体内衰老细胞堆积较多的女性中,D+Q能更好的发挥作用,增加骨密度,减少骨质流失[9]。
D+Q中的Q,也就是槲皮素是一种日常生活中就能获得的营养素,主要存在于茶叶、水果和深绿色蔬菜中。
D+Q中的达沙替尼目前还是一种处方药,我们可能暂时无法以延寿为目的使用。但基于梅奥医学中心希诺裂技术的新一代衰老抑制剂SRN-901已经展示出了惊人的效果,据赛诺根披露的实验数据显示,在针对中年小鼠(相当于50多岁人类)的衰老干预实验中,SRN-901试验组中年小鼠的剩余寿命显著提升。
《自然》杂志在给今年去世的细胞衰老先驱海弗里克写的讣告里是这样评价他的:“他一直活跃在相关领域——在许多人看来这早已过了退休年龄。”
希望无论是我们的细胞还是人生,都能逆转衰老。
作者 | 南风
编辑 | 玛洛恩
参考资料:
[1] Reed R, Miwa S. Cellular senescence and ageing. Sub-cellular Biochemistry/ Subcellular Biochemistry. January 2023:139-173.
[2] Li X, Li C, Zhang W, Wang Y, Qian P, Huang H. Inflammation and aging: signaling pathways and intervention therapies. Signal Transduction and Targeted Therapy. 2023;8(1).
[3] Ming X, Yang Z, Huang Y, et al. A chimeric peptide promotes immune surveillance of senescent cells in injury, fibrosis, tumorigenesis and aging. Nature Aging. December 2024.
[4] Zhu Y, Tchkonia T, Pirtskhalava T, et al. The Achilles’ heel of senescent cells: from transcriptome to senolytic drugs. Aging Cell. 2015;14(4):644-658.
[5] Kirkland JL, Tchkonia T. Senolytic drugs: from discovery to translation. Journal of Internal Medicine. 2020;288(5):518-536.
[6] Yao M, Wei Z, Nielsen JS, et al. Senolytic therapy preserves blood-brain barrier integrity and promotes microglia homeostasis in a tauopathy model. Neurobiology of Disease. October 2024:106711.
[7] De Oliveira Silva T, Lunardon G, Lino CA, et al. Senescent cell depletion alleviates obesity-related metabolic and cardiac disorders. Molecular Metabolism. 2024;91:102065.
[8] Scalise M, Cianflone E, Quercia C, et al. Senolytics rejuvenate aging cardiomyopathy in human cardiac organoids. Mechanisms of Ageing and Development. November 2024:112007.
[9] Farr JN, Atkinson EJ, Achenbach SJ, et al. Effects of intermittent senolytic therapy on bone metabolism in postmenopausal women: a phase 2 randomized controlled trial. Nature Medicine. 2024;30(9):2605-2612.
