COVID-19大流行后,身边好多朋友都说自己变得容易感冒、容易过敏,仿佛免疫系统经历一场恶战后老了几岁。虽然不一定是COVID-19的锅,但随着年龄的增长,我们的免疫系统会逐渐失去原有的活力,变得更容易受到外界病原的侵袭,这是事实。甚至在自身没有明确的感染源时,免疫系统也会出现过度的反应,长期下去还会导致慢性炎症和各种与年龄相关的疾病,如心血管疾病、神经退行性疾病等。
可以说,免疫系统的重要性一点也不亚于大脑。为了改善免疫系统的功能,科学家们一直在寻找解决方案。
近日,《自然·衰老》期刊发布的一项突破性研究表明,连续补充4周尿石素A(Urolithin A,简称UA)补充剂可以有效逆转免疫衰老的现象,提升免疫系统的健康[1]。

什么是免疫衰老?
免疫衰老(Immunosenescence)是指随着年龄增长,免疫系统发生的一系列功能衰退和结构改变。具体表现为,免疫系统的细胞功能下降,免疫反应的效率降低,且对新感染的反应变得迟缓。
免疫衰老的最显著特征之一是胸腺的萎缩,胸腺是产生T细胞的主要场所。随着胸腺输出的减少,体内的新型T细胞数量大幅下降,而记忆T细胞的比例却增加[2]。这种变化意味着免疫系统在面对新病原时的适应能力下降,同时可能导致对已有病毒或细菌的免疫记忆过度增强,形成慢性低度炎症状态[2,3]。
这种慢性低度炎症被称为“炎症老化”(Inflammaging),它是一种潜在的、长期激活的促炎反应,导致体内的炎症因子升高,进而增加心血管疾病、糖尿病、神经退行性疾病、甚至癌症等多种与衰老相关疾病的发生风险[5,6]。
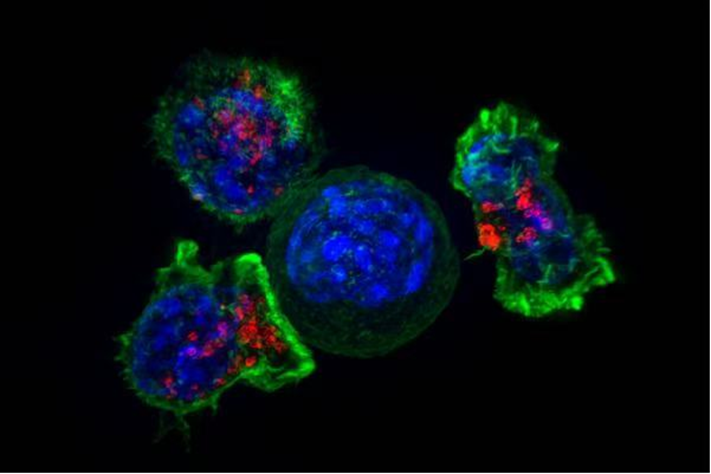
干预免疫衰老的核心——线粒体
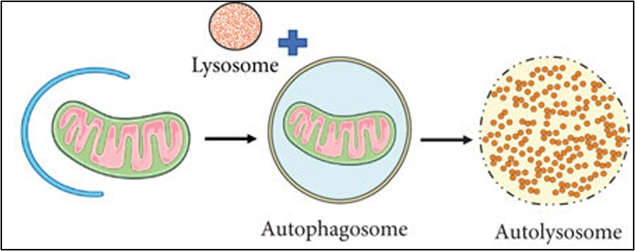
线粒体是细胞的“能量工厂”,它们负责产生能量供细胞使用。线粒体对于维持细胞功能十分重要,这是因为线粒体可以诱导细胞选择性清除受损或多余的线粒体,这个过程被称为“线粒体自噬”。
随着年龄的增长,线粒体自噬功能逐渐下降,功能失调的线粒体会逐渐积累,免疫细胞的功能也会受到影响。所以提升线粒体的质量,可以改善免疫功能、并积极影响以免疫反应功能失调为特征的衰老相关疾病。
而尿石素A正是科学界公认的首个具有促进线粒体自噬功能的天然化合物。因此,研究人员决定探索一下尿石素A对于免疫衰老的干预效果如何。
尿石素A能抵抗免疫衰老
尿石素A由肠道微生物将石榴中的鞣酸类物质转化而来的。石榴、覆盆子和红酒等食物都富含鞣酸类天然化合物。
尿石素A能促进线粒体自噬和新生,增强细胞的能量代谢,这一机制使得尿石素A成为研究免疫衰老和抗衰老的重要化合物。
先前的研究显示,补充尿石素 A 可以改善老年人的肌肉功能[8],对心血管健康也颇有益处[9]。
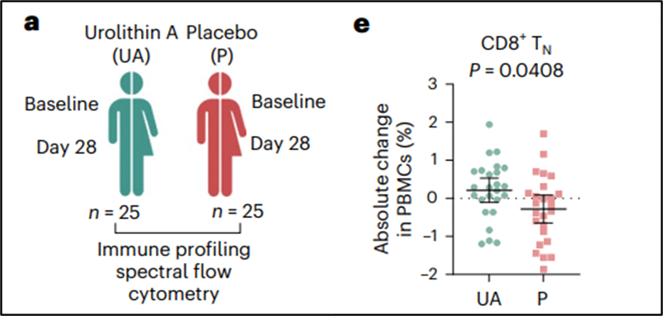
在这项新试验中,研究者招募了50名年龄在45至70岁的健康成年人。其中一半服用1000毫克尿石素A,另一半服用安慰剂,持续四周后,科学家们在分析两组受试者的免疫细胞时,有了喜人的发现:
免疫细胞数量增加
首先,UA治疗的参与者体内,初始CD8+ T细胞显著增加,这类细胞的数量往往随着年龄增长而下降。而且这些细胞中, T细胞衰竭的关键调控因子TOX的表达降低,细胞增殖标志物Ki-67的表达增加,这说明免疫细胞开始变得更年轻、更有活力。
改善免疫细胞代谢
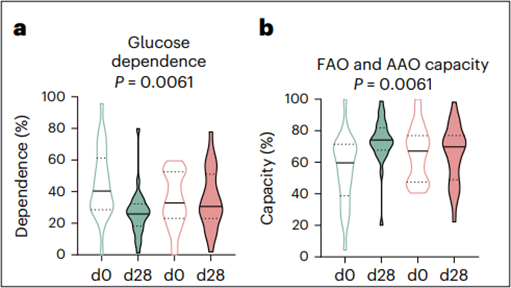
除此之外,接受UA治疗的参与者的CD8+ T细胞显示出更强的脂肪酸氧化和氨基酸氧化能力,对葡萄糖的依赖性降低——这也是免疫细胞更健康的标志。同时,研究者在这些细胞中观察到PGC-1α的表达增加,PGC-1α是线粒体生物合成的重要调控因子,表明新的健康线粒体正在取代受损的线粒体。
提升免疫应答质量
在模拟感染的实验中,尿石素A组的T细胞在激活后能更有效地产生肿瘤坏死因子(TNF),而未过度分泌IL-4。这表明尿石素A优化了免疫应答的“质量”,促进有益的1型炎症反应,避免向有害的2型炎症偏移。
![null 在补充UA和安慰剂前后CD8细胞中TNF的表达(参考资料[1])](https://cms.changshou.com/admin/static/js/ueditor/php/../attached/image/20251128/20251128185805_46749.png)
如何补充尿石素A?
想补充尿石素A,狂吃石榴就可以了吧?要是这么简单就好了。
尽管尿石素A在许多食物中有一定的存在,但由于每个人的肠道微生物群组成不同,因此转化效率也存在差异。研究表明,只有约40%的人能够通过食用富含鞣酸的食物,如石榴,产生足够的尿石素A[10]。
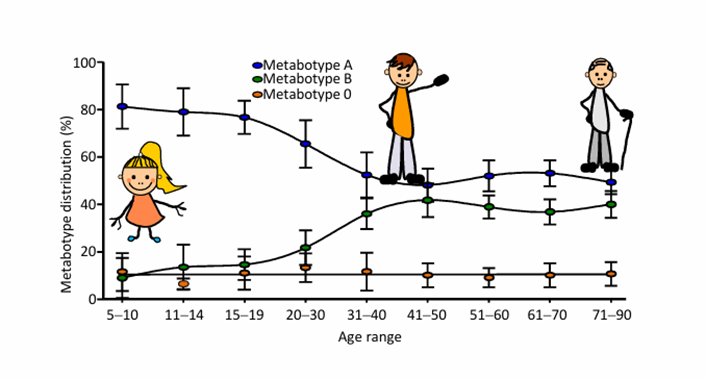
而且,随着年龄增长,从40岁左右开始,肠道菌群多样性下降,UA生成量也会断崖式减少[6]。
因此,单纯依赖食物补充尿石素A可能无法达到理想的效果,尤其对于40岁以上人群来说,成品尿石素A补充剂才是最高效的选择。
根据现有临床数据报告,每天摄入250~1000 毫克尿石素 A是相对安全的,但有基础疾病或长期服药的人群如需服用,请咨询专业人士的意见。
关于尿石素A的详细内容,请见《长寿指南:尿石素A(Urolithin A):功效与作用、安全性和服用方法》。
参考资料:
[1] Denk, D. et al. Effect of the mitophagy inducer urolithin A on age-related immune decline: a randomized, placebo-controlled trial. Nature Aging 5, 2309–2322 (2025).
[2]Sun, L., Su, Y., Jiao, A., Wang, X., & Zhang, B. (2023). T cells in health and disease. Signal Transduction and Targeted Therapy, 8(1), 1-50.
[3]Swain, A. C., & Borghans, J. A. (2022). Effect of cellular aging on memory T-cell homeostasis. Frontiers in Immunology, 13, 947242.
[4]Cortés-Martín, A. et al. The gut microbiota urolithin metabotypes revisited: the human metabolism of ellagic acid is mainly determined by aging. Food & Function 9, 4100–4106 (2018).
[5] Hotamisligil, G. S. Inflammation, metaflammation and immunometabolic disorders. Nature 542, 177–185 (2017).
[6] Park, E. J. et al. Dietary and genetic obesity promote liver inflammation and tumorigenesis by enhancing IL-6 and TNF expression. Cell 140, 197–208 (2010).
[7] Shao, R., Li, J., Qu, T., Liao, Y. & Chen, M. Mitophagy: a potential target for Pressure Overload‐Induced Cardiac Remodelling. Oxidative Medicine and Cellular Longevity 2022, 2849985 (2022).
[8] Singh, A. et al. Urolithin A improves muscle strength, exercise performance, and biomarkers of mitochondrial health in a randomized trial in middle-aged adults. Cell Reports Medicine 3, 100633 (2022).
[9] Selma, M. V. et al. The gut microbiota metabolism of pomegranate or walnut ellagitannins yields two urolithin-metabotypes that correlate with cardiometabolic risk biomarkers: Comparison between normoweight, overweight-obesity and metabolic syndrome. Clinical Nutrition 37, 897–905 (2017).
[10] Singh, A., et al. (2021). Direct supplementation with Urolithin A overcomes limitations of dietary exposure and gut microbiome variability in healthy adults to achieve consistent levels across the population. European Journal of Clinical Nutrition, 76(2), 297–308.
