你有没有过这样的感觉:年纪大了以后,感冒恢复得更慢,流感疫苗打了也还是中招,甚至一场小病要拖上很久才好?这不是你的错觉。免疫系统的确会随着年龄增长而衰退,这种现象在科学上叫做免疫衰老。
免疫衰老不只是让人更容易生病,老化的免疫系统还会反过来加速全身器官的衰退。去年,美国斯坦福大学的科研人员发现,在长达17年的追踪中,大脑和免疫系统同时保持“年轻”的群体死亡率仅为3.8%,而普通人是7.92%[1]。
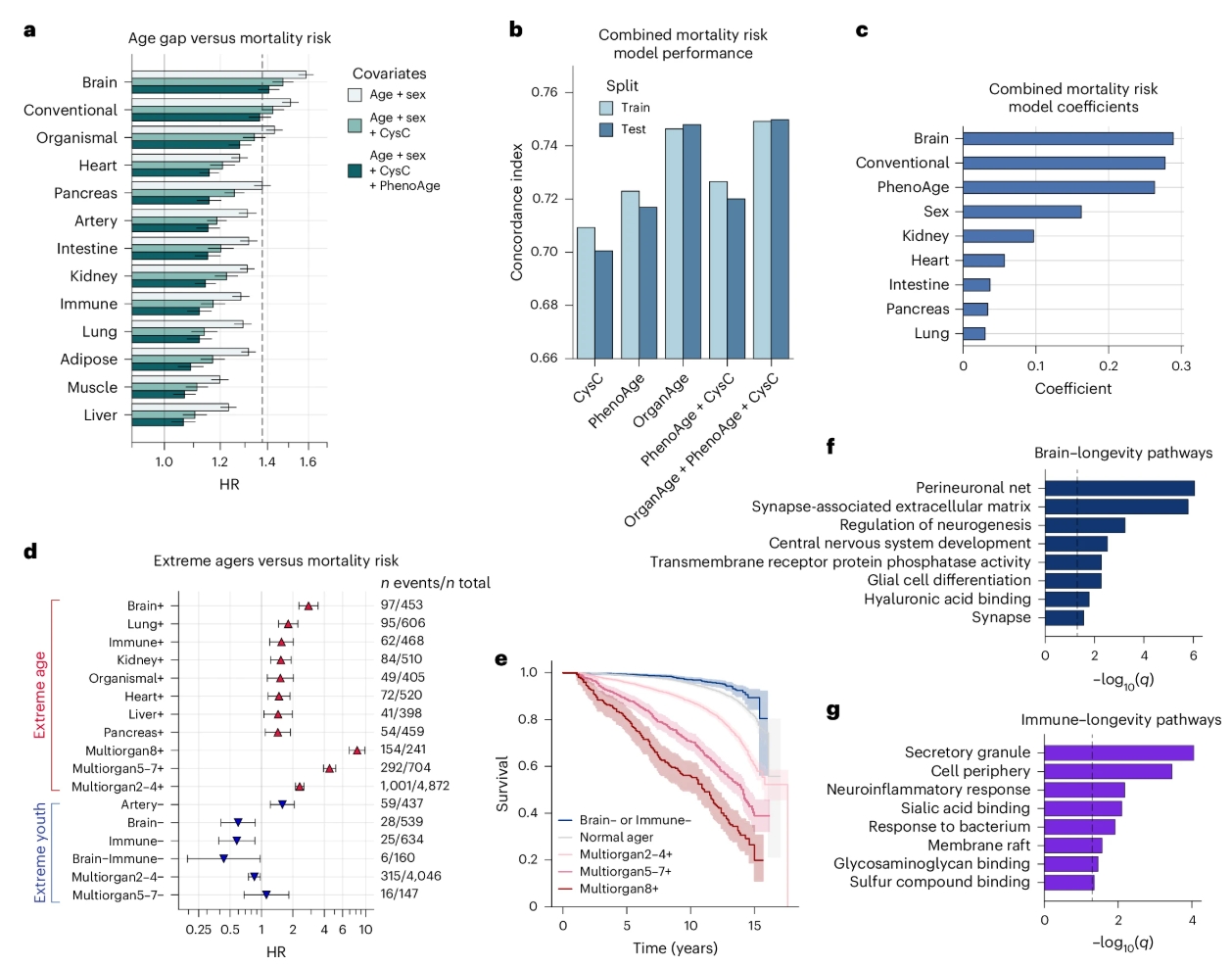
那么,免疫系统到底是怎么老的?能准确衡量吗?有没有办法“踩一脚刹车”?

近日,中国科学院国家生物信息中心张维绮团队、动物研究所刘光慧团队等合作在《Immunity》期刊发表了一项研究,利用230名20至84岁健康志愿者的外周血,分析了将近120万个免疫细胞,构建了一套“人类免疫衰老时钟”,并从中找到了一个关键的调控因子——RUNX1[2]。
免疫衰老的三个典型特征
要研究免疫衰老,首先得看清它长什么样。研究者招募了230名来自浙江衢州的20-84岁的健康人,排除了有严重慢性病、不良生活习惯的个体后,对近120万个外周血单个核细胞进行了单细胞RNA测序和T细胞受体测序,精细绘制了24种免疫细胞亚型的图谱。
对比老年组(60-69岁)和年轻组(20-29岁),他们发现了三个明显的变化。
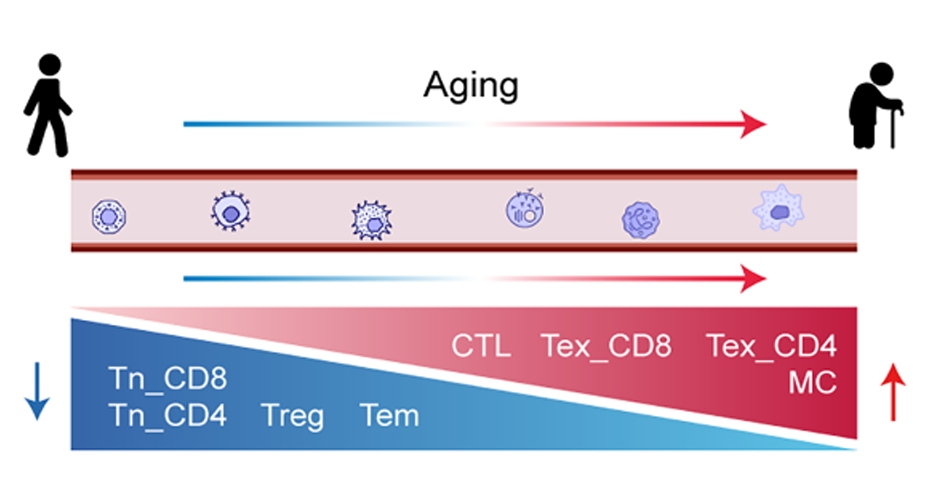
幼稚T细胞大幅减少
幼稚T细胞是免疫系统的“新兵”,尚未遇到过抗原,可以随时分化为各种效应细胞。数据表明,无论是CD4+还是CD8+的幼稚T细胞,其比例都随年龄显著下降。与此同时,中央记忆T细胞和终末耗竭T细胞的比例上升,说明免疫系统的“人才储备”正在枯竭。
衰老标志物积累
老年组细胞中,一种叫SPIDER-βGal的衰老染色阳性细胞变多了,DNA损伤标志物γ-H2A.X升高,而维持基因组稳定性的异染色质标志H3K9me3则下降了。这些是细胞层面“变老”的直接证据。
慢性炎症信号增强
单核细胞(一种与炎症相关的免疫细胞)在老年组中比例上升,同时血浆中的补体激活和炎症相关蛋白水平也更高。这印证了“炎性衰老”的概念——年纪越大,身体越处于一种低度的慢性炎症状态。
中年40岁,免疫系统处在一个“弯道拐点”
如何量化免疫衰老?研究者利用机器学习方法,建立了多套“免疫时钟”模型。在所有时钟里,表现最好的那些基本上都是T细胞模型,说明T细胞确实是免疫衰老中最敏感、最关键的指示器。换句话讲,想知道一个人的免疫系统老没老、老了多少,盯着T细胞就够了。
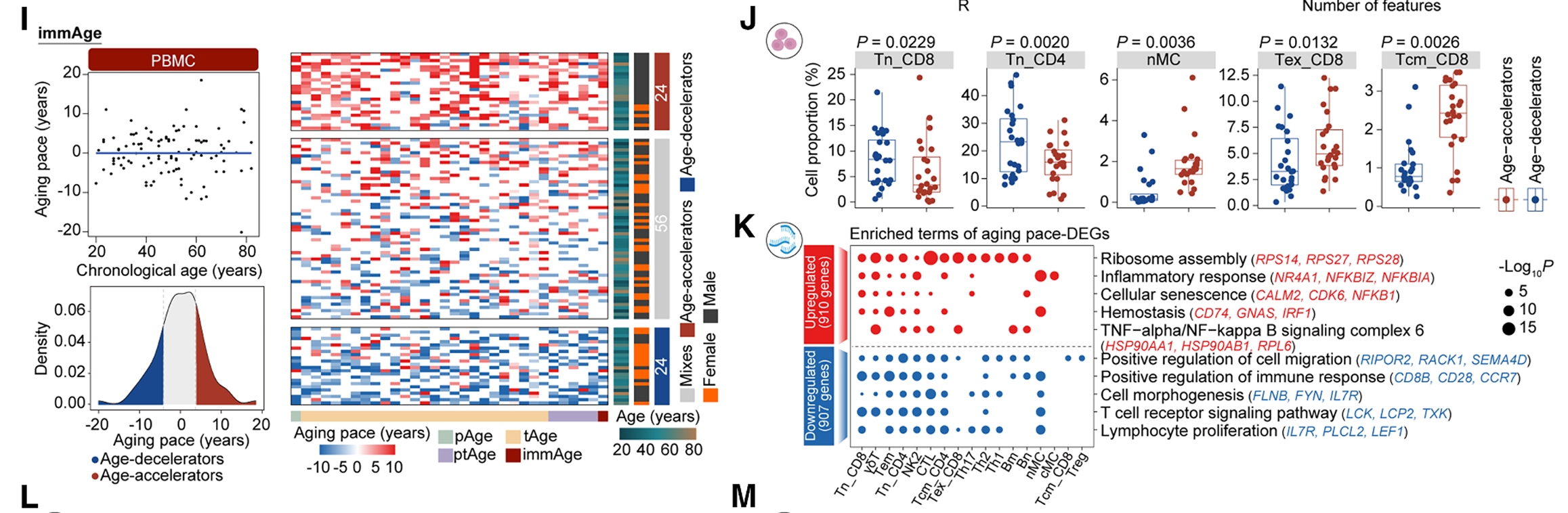
值得注意的是,免疫衰老并不是匀速发生的。研究团队在动态模型中发现,免疫系统在40岁左右出现了明显的细胞组成和转录组重编程高峰。换句话说,中年是免疫系统“加速衰老”的一个关键转折期。如果这个阶段能主动干预,可能就是最理想的窗口期。
人过四十,胸腺早已开始萎缩,没那么多新造的初始T细胞补充到一线,剩下的T细胞面对层出不穷的刺激逐渐“杀不动”了,耗竭型T细胞比例越来越高,而单核细胞的比例却在增加,其后果就是全身性的慢性炎症。
研究还进一步将这个“免疫年龄”的评估下沉到了个人层面。团队定义了免疫衰老速率,即预测的免疫年龄与实际年龄之间的差值。根据这个指标,他们把人群分成了加速衰老组和减速衰老组。
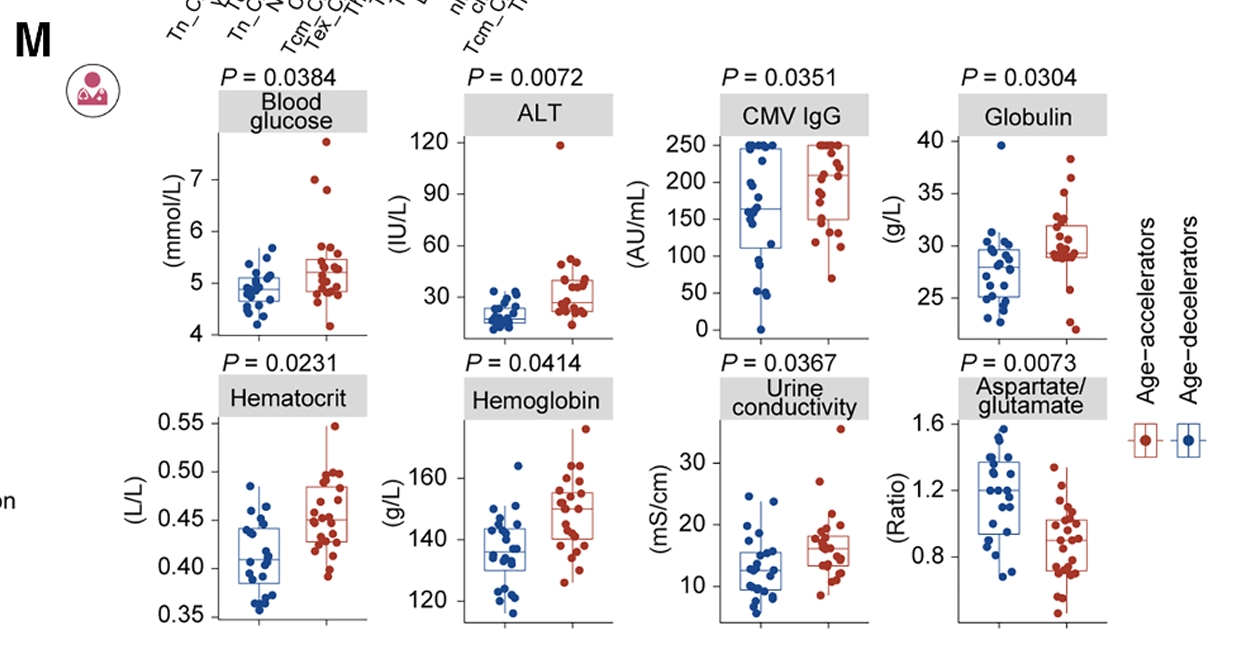
减速衰老组的人免疫图谱更年轻,保留了更多的初始T细胞、更少的耗竭T细胞,转录组里衰老标志和炎症信号更低,血浆里的代谢物也更倾向于抗炎、抗氧化。更重要的是,这些人确实有更优越的生理机能:血糖控制更好、肝功能指标(ALT)更低、心肺储备能力更强。
换句话说,免疫衰老的“快慢”与全身多个器官系统的健康状况是耦合的。免疫系统不只是一道防线,它也是反映整体生理状态的一面镜子。
RUNX1:被免疫时钟找出来的衰老“刹车”
既然T细胞是免疫衰老的核心驱动力,那么在T细胞内部,谁是调控衰老的关键分子?研究者把免疫时钟中权重最高的基因拎出来,做了系统的基因调控网络分析,最终锁定了转录因子RUNX1。在各种T细胞中,RUNX1的蛋白表达水平都随年龄增长显著下降。
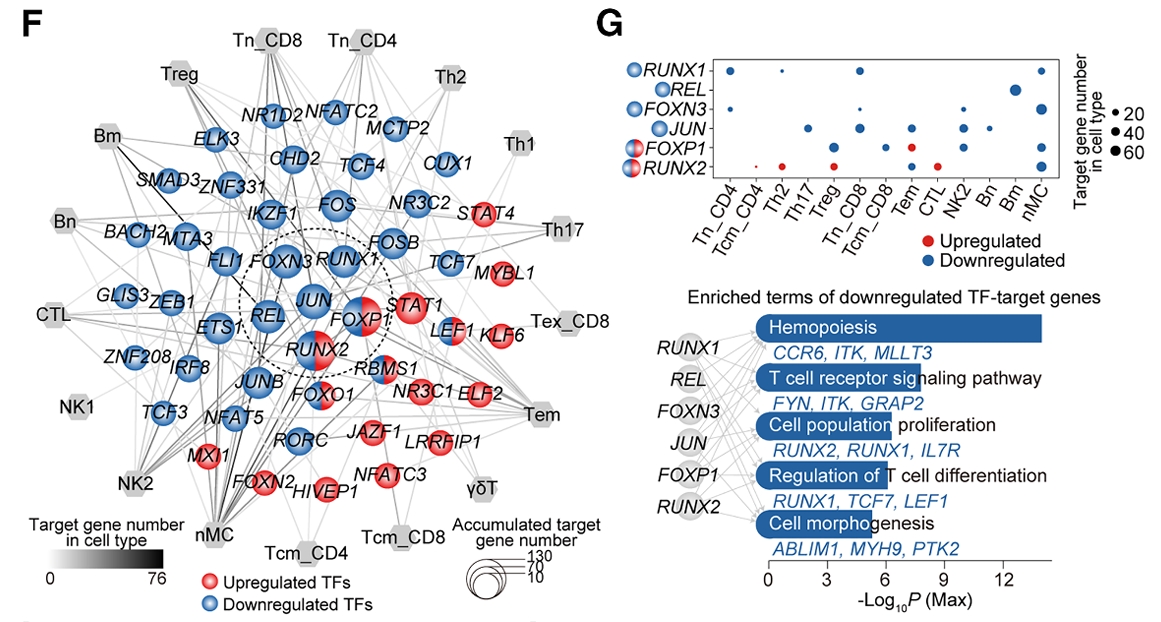
那么,RUNX1到底在T细胞里干什么?
研究者做了一系列功能实验。首先在年轻人的T细胞里把RUNX1“敲掉”。没了RUNX1之后,T细胞很快表现出典型的衰老特征:细胞周期抑制蛋白p21大量表达,细胞增殖能力急转直下,衰老相关的分泌表型基因被激活,CD8+ T细胞的端粒明显缩短,细胞毒性也大不如前。
这一连串变化形成了证据闭环:RUNX1下降,T细胞迅速衰老。
接下来是反向实验——在老年人的T细胞里强行过表达RUNX1。结果恰好反过来:细胞衰老标志物的表达下降,恢复共刺激分子CD27(一个关系到T细胞活化和记忆力的重要受体)的表达,端粒也显著延长。在CD8+ T细胞上,恢复RUNX1还能重新激活细胞毒性功能,还原出相当可观的杀伤力。作为关键的分子验证,研究者还观察到,T细胞“干性”的维持因子TCF7,也在RUNX1过表达后被重新激活。
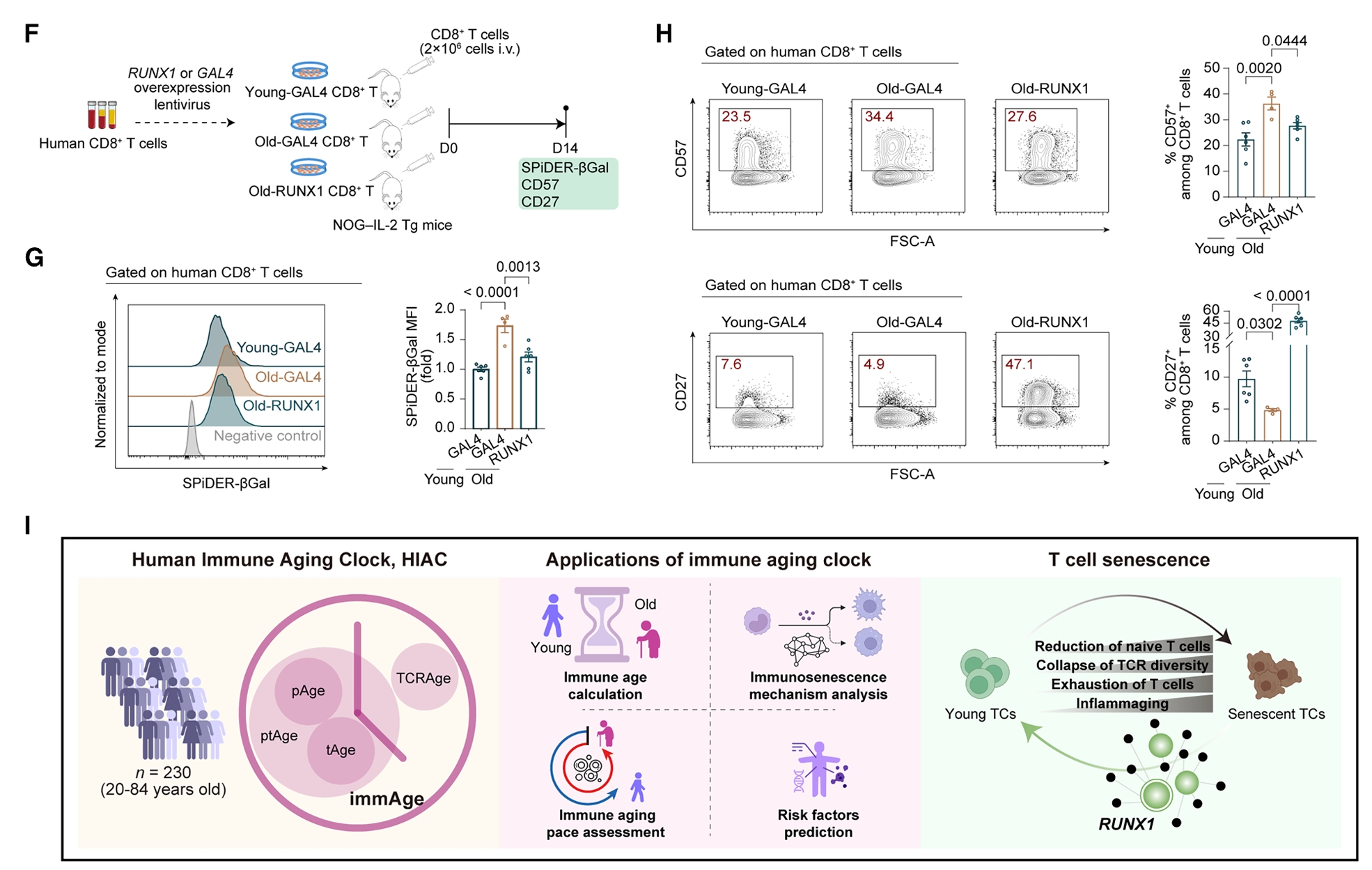
为了检验RUNX1的保护作用是否能在真正的活体环境中站住脚,研究者把过表达RUNX1的老年人T细胞移植到了免疫缺陷的NOG-IL-2 Tg人源化小鼠体内。转移两周后,这些过表达RUNX1的T细胞仍然维持着较低的衰老标志物水平和较高的活化功能。
简单来说,RUNX1像一个“总开关”,通过直接结合并激活一批维持T细胞年轻态的基因,来抵抗衰老程序的启动。
不是万能的,但打开了一扇窗
当然,研究也有它的边界。这是一项横断面研究,所有样本都来自浙江衢州地区,结果能不能推广到不同人种和更广泛的人群,还需要在不同地理和种族背景的队列里进一步验证。另外,RUNX1下调的上游机制是什么,是哪些因素导致它在T细胞中随年龄下降的,目前仍不清楚,这将是下一步研究的重要方向。
那在等科学家的下一步成果之前,我们自己能做点什么?

虽然RUNX1暂时还不能通过“吃点什么”或“补点什么”来直接提升,但免疫衰老的整体节奏,很大程度上是可以被生活方式调节的。
1.规律的中等强度有氧运动(比如快走、慢跑、骑车)能显著降低老年人体内的慢性炎症水平,延缓T细胞耗竭。
2.充足的睡眠也至关重要——长期睡眠不足6小时的人群,其免疫细胞功能下降的速度明显加快。
3.控制体重、减少精制糖和加工食品的摄入,有助于避免持续的代谢性炎症状态。
4.接种疫苗(流感疫苗、肺炎疫苗、带状疱疹疫苗) 则是目前最直接的“免疫系统保养”手段,尤其对老年人来说,能有效降低感染风险和后续的全身性炎症冲击。
虽然这些方法有点老生常谈,但恰恰是目前证据最充分的“免疫减速法”。科学家在找开关,我们可以先管好旋钮。也许在不久的将来,定期“保养”一下T细胞,会像打疫苗一样成为常规的老年健康管理手段。
参考资料:
[1] Oh HSH, Guen YL, Rappoport N, et al. Plasma proteomics links brain and immune system aging with healthspan and longevity. Nature Medicine. 2025;31(8):2703-2711. doi:10.1038/s41591-025-03798-1
[2] Ping J, Qiao Q, Gao DD, et al. Human immune aging clock identifies RUNX1 as a decelerator of T cell senescence. Immunity. 2026;59(4):1039-1057.e11. doi:10.1016/j.immuni.2026.02.007
