人到中年的某一时刻,你可能会突然发现自己体力变差了,体检报告上多了几个加号,睡眠也变少了——这可能不是错觉,因为近年来关于衰老最震撼的研究结果之一就是:衰老不是匀速直线,而是像阶梯一样,在某个时间点突然发生的。 这些研究大部分是基于人类生物样本的组学研究,这种方法的局限是,只能研究较短时间段内的变化,难以追踪单个样本的生命全周期。毕竟从一个人出生开始就定期对其进行样本收集,并持续到死亡,基本是不可能完成的任务。 因此科学家把视线转向了生命周期较短,但是和人类有足够相似性的脊椎动物非洲青鳉鱼(Nothobranchius furzeri)。斯坦福大学用其完成了第一个对脊椎动物全生命周期连续追踪的研究,从行为轨迹上发现,非洲青鳉鱼的衰老也不是匀速发生的,甚至从中年时期行为上发现了能够预测剩余寿命的强大信号。 我们常见的实验室动物生命周期都不算短:小鼠的中位寿命约2年,斑马鱼约3年。用这些物种做全生命期的连续行为监测,在技术和成本上几乎不可行。研究团队选择的非洲青鳉鱼,是目前已知寿命最短的脊椎动物之一,在实验室条件下中位寿命仅4—8个月。 短寿不等于简单。青鳉鱼拥有和哺乳动物相似的复杂神经系统,在肌肉衰退、免疫功能下降、认知变化等方面展现出与人类衰老高度相似的生物学特征。对衰老研究来说,它就像是一部被压缩了的"人类衰老教材",几个月之内走完了人类几十年的历程。 研究团队由熟悉衰老领域的遗传学家和鱼类行为研究专家组成,确保能正确记录、整理和分析青鳉鱼的数据。 研究团队为81条雄性青鳉鱼各自配备了独立水箱,摄像头从鳉鱼进入性成熟期(约3—4周龄)开始,以每秒20帧的速度持续拍摄,直至每条鱼自然死亡。平均追踪时长约220天,最长的一条被追踪了371天,整个实验共产生了数百亿帧视频数据。 鱼的每一天、每个动作,都被摄像头完整记录了,接下来就是利用AI对这些海量数据进行标记。研究团队训练了模型,在每一帧图像中识别鱼身上的6个关键点——吻部、体中段、尾部等,由此总结出57种描述鱼的运动状态的姿势特征,包括速度、体形弯曲度、游动方向等。 在此基础上,研究人员进一步从这些连续运动数据中归纳出100种"行为音节",也就是鱼在日常生活中反复出现的短时行为单元,涵盖了主动行为(冲刺、翻转、倒游)和静止行为(缓慢漂移、休息)。行为音节就是鱼类行为的词典。拿人类行为举个例子,来回踱步加上挠头,可能代表焦虑;整天躺着不动,减少进食,可能代表情绪低落、抑郁等。81条鱼的生命全记录,被用这样的词典翻译好,构成了它一生的纪录片。 当然最重要的是从这个纪录片里寻找规律,判断它们的衰老轨迹。比如当运动量减少连续超过几天,就标志着它进入了衰老阶段。 大多数个体在一生中经历了2-6次行为模式的快速转变,每次转变仅持续几天,之后进入长达数周的相对稳定期。这些转变通常是单向推进的,不会在两个阶段之间来回切换。 研究者把这种衰老模型比作俄罗斯方块:很多块可以被抽走,结构不会崩塌,直到某一个关键位置被触动,于是整体开始重新排列。 这个现象和人类衰老研究相呼应,组学分析发现,人类在44岁和60岁左右会出现两个断崖式衰老,且超过80%的分子标记物表现出非线性变化模式。虽然鱼类实验使用的是行为数据,人类实验使用的是分子层面的组学研究,但从结果看,它们都描述同一种机制——衰老不是渐进的,而是断崖式的。 81条鱼的寿命差异很大,短的不到两个月,长的超过一年。尽管它们基因背景相似,生活在同样严格控制的实验环境下,但衰老轨迹从它们寿命的中年时期就开始分化。 研究团队把鱼按寿命分组,再回溯分析各组鱼在不同年龄的行为数据,发现两组的行为轨迹在约70天龄(约等于人的中年早期)时出现了显著分叉——此时鱼的体型和进食量尚无明显差异。 分叉体现在两个维度上: 活动量。到100天龄时,长寿组的自发游动显著更活跃,峰值游速也更高。这种差异不是"有没有体力运动"的问题,而是一种自发的、持续的高活跃状态,在统计上和未来寿命呈显著正相关。 这两个行为信号强大到足以让机器学习模型仅凭中年阶段几天的行为记录,就能较准确地预测个体的剩余寿命。 行为层面的分化背后,是身体内部的生物学变化。 研究团队在鳉鱼生命的不同阶段(幼年、中年、老年)对它们的8个器官进行了基因表达分析,不同寿命个体的差异最集中地出现在一个器官上:肝脏。 在短寿轨迹的鱼中,肝脏里与核糖体生物合成相关的基因群体活性显著更高——核糖体在细胞内负责合成蛋白质,这些基因的异常高活跃,意味着细胞在大量、持续地制造蛋白质。这种状态是某种代谢失衡的信号,类似一台发动机转速异常偏高,看起来充满动力,实际上是一种失控的消耗。 肝脏在代谢调控和系统性炎症中处于核心位置。已有大量衰老研究指出,肝脏的代谢失调是驱动全身慢性低度炎症的一个重要来源,而低度慢性炎症正是"衰老十二大标志"中的核心机制之一。鱼的肝脏可能最早感知到了衰老轨迹的差异,并将其写进了基因表达里。 活跃状态和睡眠节律,是这项研究中区分长短寿命最敏感的行为信号。这不是第一次在不同物种中观察到类似的关联。在人类衰老研究中,持续的规律运动已被证实能够改善线粒体功能、降低慢性炎症标志物、延缓肌肉量下降,与健康寿命的延长直接相关。而睡眠节律的紊乱——尤其是白天嗜睡增多、夜间睡眠质量下降——不仅是衰老的结果,也可能是促进衰老加速的因素。 与被监测的鳉鱼不同,人类拥有主动干预的空间。鱼只能吃被饲喂的食物,在有限的水箱里游动;而我们可以通过有意识的行为选择,来改善代谢状态和身体的衰老轨迹。用少吃精制碳水、适当增加纤维和蛋白质的饮食模式,减轻胰岛素波动;用有氧运动和力量训练结合的方式,提高胰岛素敏感度。 这项研究指出的可能性是,尽管行为数据非常容易获得,但同样能帮我们建立衰老预测模型。而今天,手机和手环已经在持续记录我们的步数、睡眠时长、活动心率。如果这些数据有一天能被纳入类似的分析框架,或许能给出比年龄数字更准确的衰老状态指示——不是告诉你"已经45岁了",而是告诉你"目前处于哪个衰老阶段,以及这个阶段是否在正常范围内"。 虽然衰老是不可避免的,断崖和阶梯也是真实存在的,但我们有能力做到的是,让断崖尽量不那么陡峭,下阶梯的时候稳稳地踩住地面。能达到这一目标最简单可行的方法,就是从今天开始建立健康、活跃的生活习惯,任何时候开始都不算晚,都能把细胞层面的获益积累到晚年。
实验是怎么进行的
选择合适的脊椎动物

研究方法
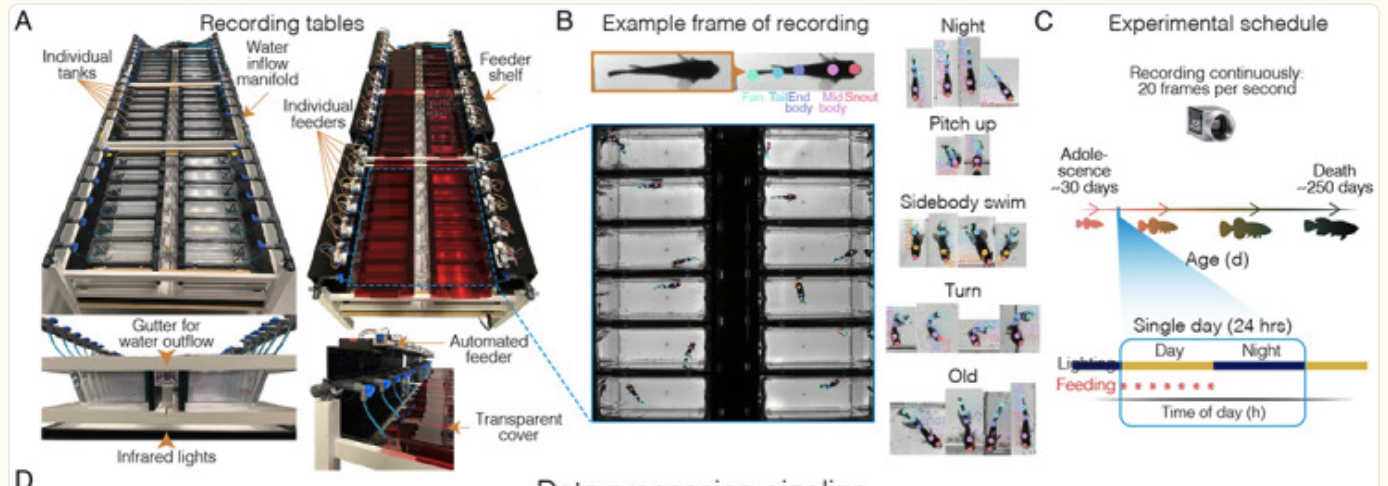
量化行为
鱼的衰老也是阶梯状的
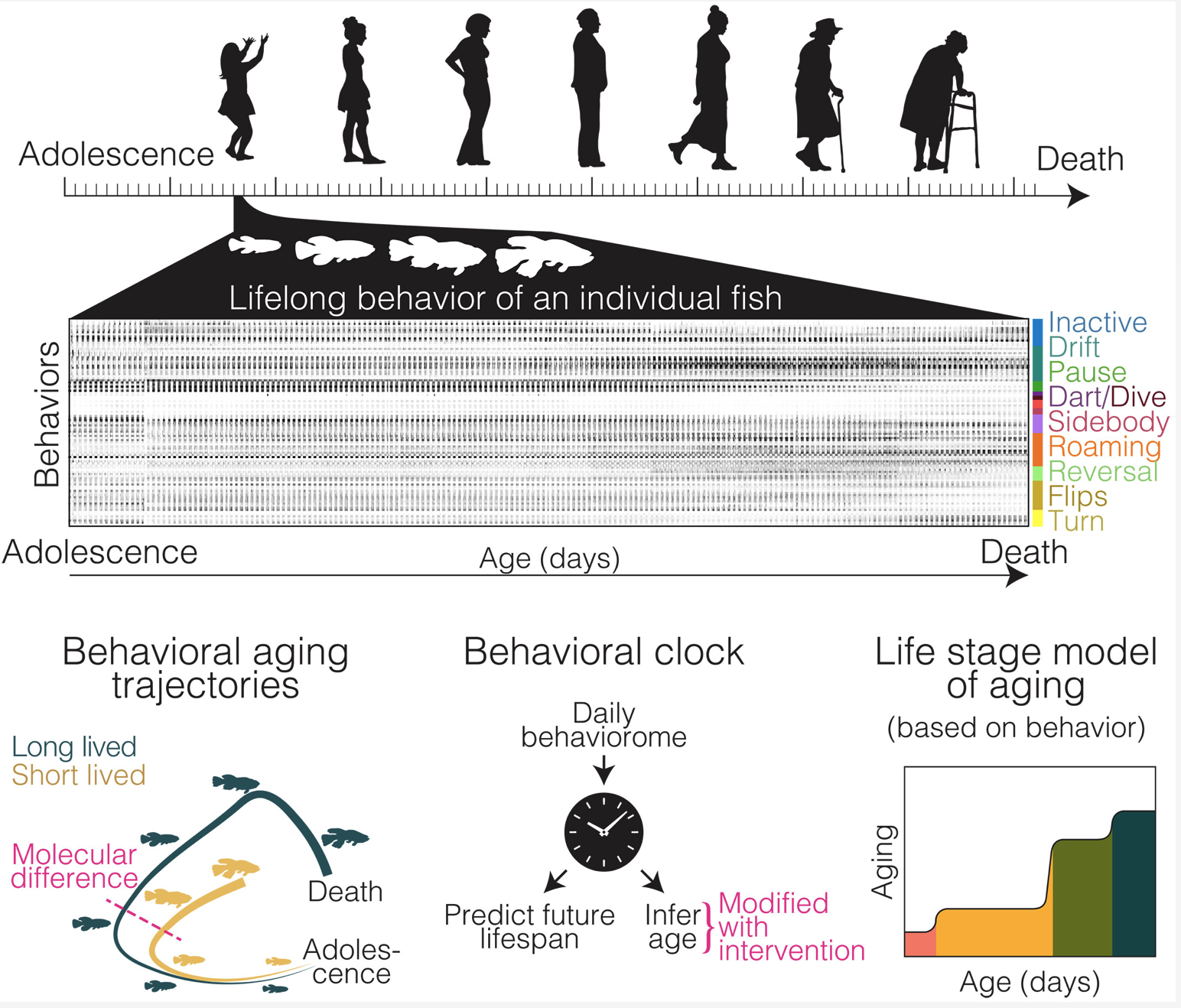
中年行为和寿命高度相关
睡眠节律。短寿组的鱼在白天的睡眠时间随年龄推移明显增多,睡眠开始蔓延进白天的活跃时段;长寿组的鱼睡眠则主要集中在夜间,白天维持更高的活跃度。肝脏在代谢调控中有重要作用
对人类有什么启发
行为习惯改变的不只是今天,还有未来
代谢健康是长寿的关键
行为学数据同样可以用来预测衰老轨迹

参考资料:
Bedbrook CN, Nath RD, Zhang L, Linderman SW, Brunet A, Deisseroth K. Lifelong behavioral screen reveals an architecture of vertebrate aging. Science. 2026;391(6790):eaea9795.
Singh PP, Demmitt BA, Nath RD, Brunet A. The genetics of aging: A vertebrate perspective. Cell. 2019;177(1):200–220.
López-Otín C, Kroemer G, Serrano M. The hallmarks of aging: 2023. Cell. 2023;186(2):243–278.
Shen X et al. Nonlinear dynamics of multi-omics profiles during human ageing. Nature Aging. 2024.
Nieman DC, Wentz LM. The compelling link between physical activity and the body's defense system. J Sport Health Sci. 2019;8(3):201–217.
