你有没有想过,为什么我们总是用“岁月不饶人”来形容衰老?时间似乎是一条单行道,我们只能被动地接受它的痕迹。但科学家的探索却一次次挑战这个直觉:如果把年轻小鼠和年老小鼠的血管连接起来,年老小鼠的肌肉和大脑竟然会“恢复活力”[1],甚至还可以延长老年小鼠的寿命[7]。
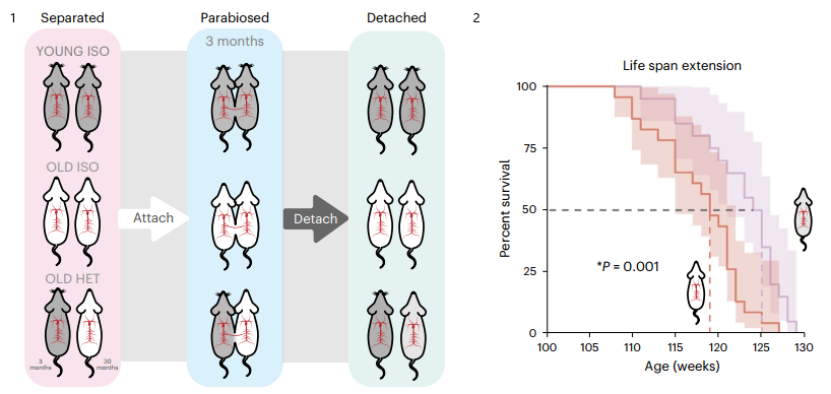
然而,小鼠实验的结果很难直接推演到人类身上。我们不可能像连接小鼠那样连接两个人的血管,也不可能花几十年等待一个人慢慢变老来观察实验效果。那么,有没有一种更快、更接近人类生理的方法来研究衰老?

美国加州大学伯克利分校的研究团队近日发表的一项研究给出了一个巧妙的设计:在指甲盖大小的芯片上,用人类细胞“造”出一个会衰老的微缩系统[2],不仅能快速诱导衰老特征,还完成了多种衰老干预策略的验证,并找到了“最优解”。
一个微缩的“脂肪-肝脏轴”
研究者使用的是一种被称为“器官芯片”的技术。所谓器官芯片,并非将整个器官缩小,而是将功能细胞放置在模拟人体内环境与结构的微流控芯片上。
研究团队选用了两种对人类代谢至关重要的细胞:白色脂肪细胞和肝细胞。这两种细胞都源自人类诱导多能干细胞(hiPSC)——先将成体细胞(如皮肤细胞)重编程为具有分化潜能的干细胞,再定向诱导分化而成。所有细胞均来自同一名男性健康供体,这样能确保后续观察到的差异主要由外部因素(如血清)引起,而非个体遗传背景差异。
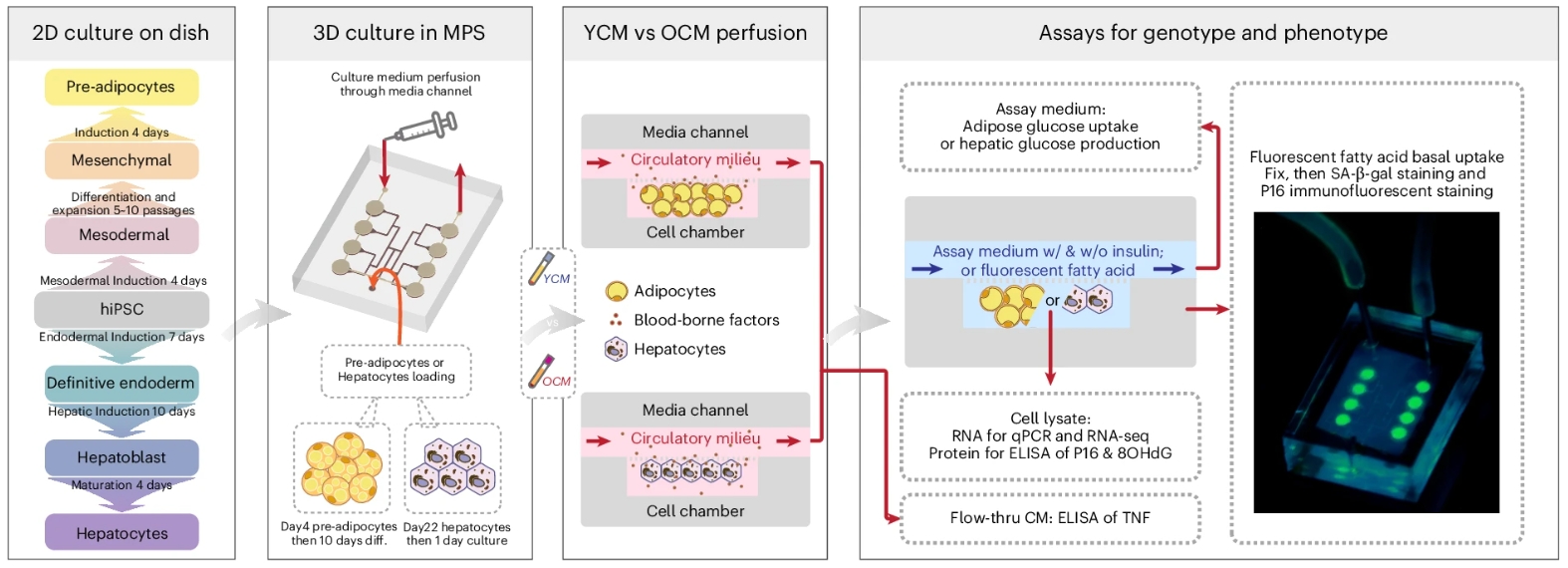
芯片设计包含两个独立的细胞培养腔室,分别装载脂肪细胞和肝细胞。两个腔室之间有微流控通道相连,模拟人体内的门静脉系统——脂肪组织分泌的因子会通过这个通道直接流向肝脏。这个设计并非随意为之,因为在人体内,内脏脂肪释放的物质确实会通过门静脉首先到达肝脏,直接影响其功能。
研究的关键在于灌注到芯片中的培养基成分。它不是普通培养液,而是加入了5%的人类血清。这些血清来自两组健康捐献者:一组是21-34岁的年轻人,另一组是62岁以上的老年人。研究者分别称之为“年轻循环环境(YCM)”和“老年循环环境(OCM)”。
整个实验要回答的问题是:仅仅是循环环境(血液)的不同,会让这些“年轻”的细胞发生什么变化?
4天,衰老特征全面出现
结果出乎意料的快。仅仅4天后,那些被老年血清处理的脂肪和肝脏芯片,就表现出了一系列典型的衰老特征。
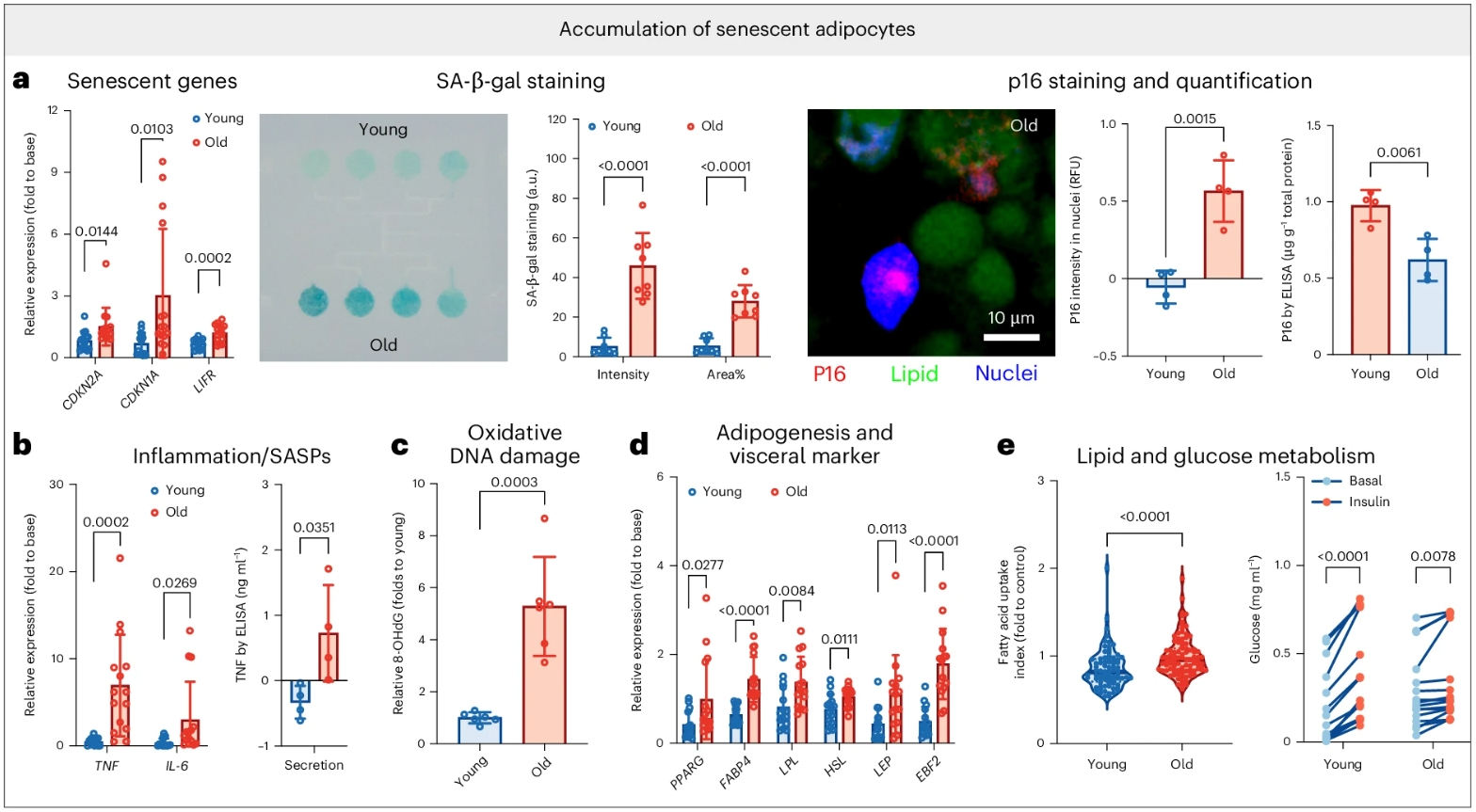
首先是细胞衰老本身。芯片中的细胞大量进入“退休”状态,不再正常分裂和发挥作用。研究者检测到衰老相关基因CDKN2A(编码p16蛋白)的表达显著上升,同时,细胞开始分泌大量炎症因子,如白细胞介素-6(IL-6)和肿瘤坏死因子(TNF),即“衰老相关分泌表型(SASP)”[3]。
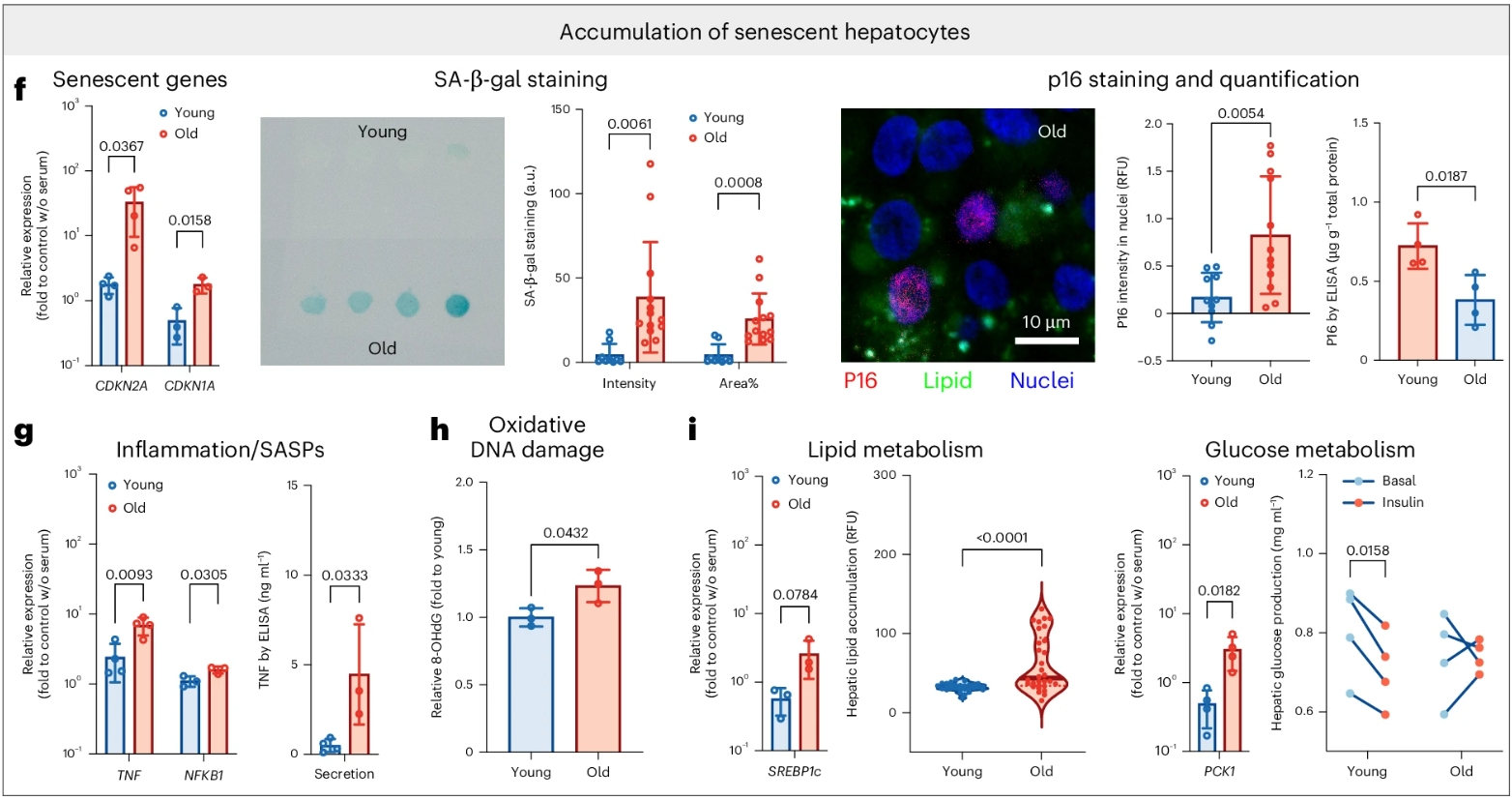
其次是代谢紊乱。芯片上的脂肪细胞和肝细胞对胰岛素的反应变得迟钝——胰岛素敏感性下降,是2型糖尿病的前兆。脂肪细胞摄取葡萄糖的能力减弱,肝脏的葡萄糖生成调控失常,同时,细胞内的氧化DNA损伤水平也开始升高。
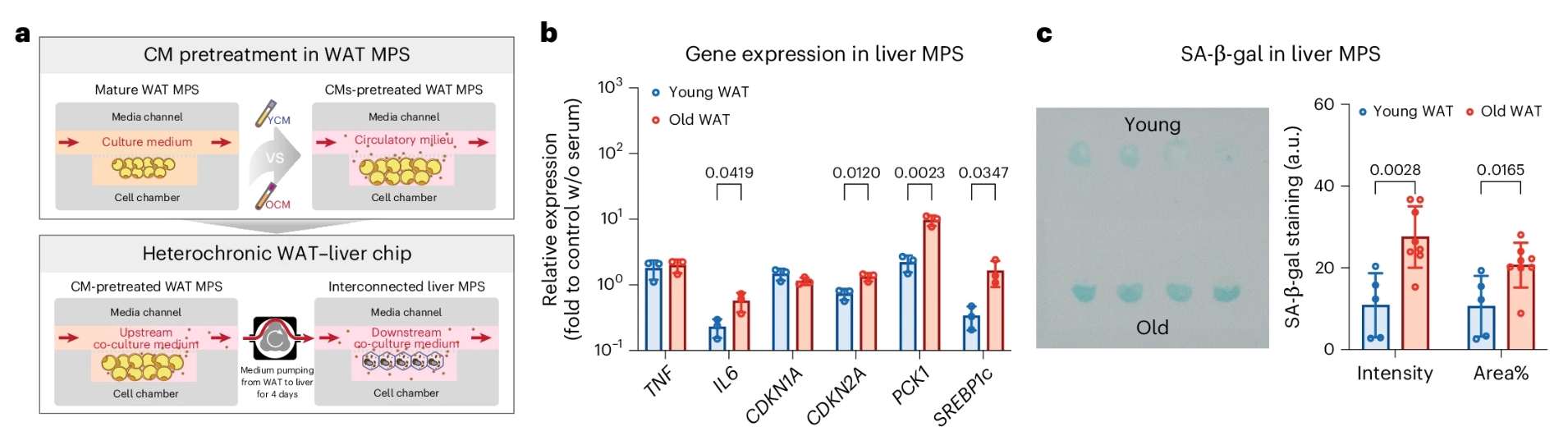
有趣的是,研究发现,这种衰老具有“传染性”。研究者先让脂肪芯片暴露于老年血清4天,然后将其与一个未经处理的肝脏芯片连接起来,只灌注普通培养液(不含任何血清)。结果发现,这个被“衰老”的脂肪,竟然能诱导肝脏芯片也出现衰老和功能障碍:细胞炎症水平升高、胰岛素抵抗加剧、脂肪堆积增加。也就是说,衰老的脂肪组织会通过其分泌的因子,将衰老信号传递给下游器官。
转录组学验证:芯片衰老与真实人类衰老高度一致
仅凭几个衰老标志物还不够有说服力。研究者对芯片上的细胞进行了RNA测序,分析其基因表达谱,并与GTEx数据库中真实人类脂肪组织的基因表达数据进行了系统比较。GTEx项目收集了来自数百名不同年龄供体的多种组织样本,是目前最大规模的人类组织基因表达数据库之一[4]。
分析结果显示,被老年血清处理4天的芯片细胞,其基因表达模式与GTEx数据库中60-69岁老年人的皮下脂肪组织高度一致;而被年轻血清处理的芯片细胞,其表达模式则与20-29岁的年轻人相似。
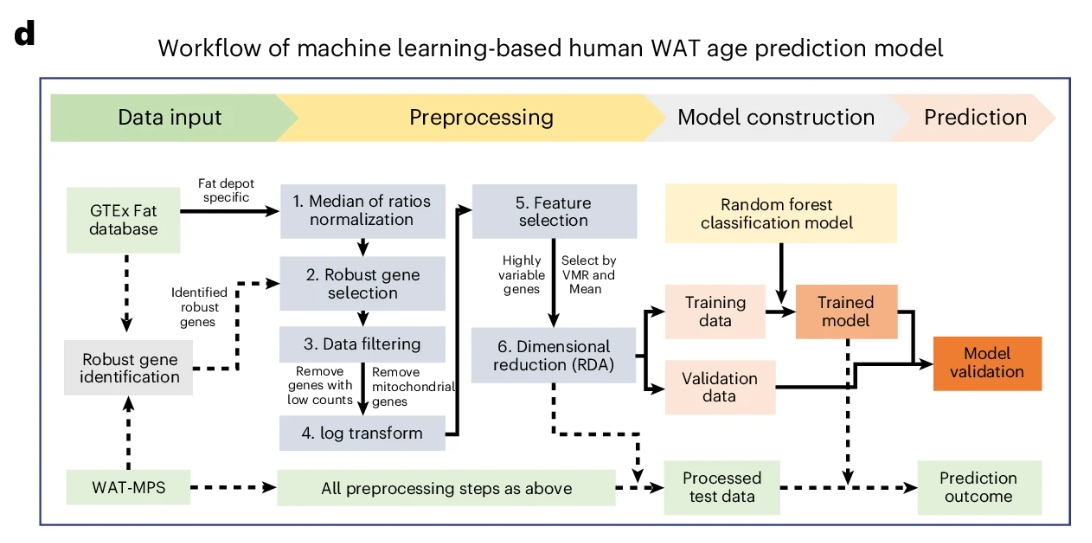
为了进一步量化这种相似性,研究者利用GTEx数据训练了一个机器学习模型,用于预测组织的“生物学年龄”。模型的训练基于70%的GTEx数据,在剩余30%数据上验证时,准确率达到90%以上。将这个模型应用于芯片数据后,结果非常直观:
被年轻血清处理的芯片 → 模型预测年龄与年轻捐献者一致;
被老年血清处理的芯片 → 模型预测年龄迅速攀升至与老年捐献者相当的水平。
换言之,芯片上细胞的“生物学年龄”主要由循环环境(血清)决定,而非培养时间的长短。衰老,在某种程度上,可以被视为一种循环环境病——只要把你泡在“衰老的血液”里,你的细胞就会迅速老去。
逆转衰老:谁是最有效的“解药”?
既然老年血清能让细胞变老,那换成年轻血清能逆转这个过程吗?如果能,哪些药物能帮忙?研究者测试了五种干预策略:
达沙替尼+槲皮素(D+Q):一种“抗衰老药”,专门清除衰老细胞;
TGF-β信号通路抑制剂(ALKSi):阻断一个在衰老中过度活跃的信号通路;
催产素:一种与社交、分娩有关的激素,在小鼠研究中显示出抗衰老效果[5];
雷帕霉素:经典的mTOR抑制剂,被广泛研究的寿命延长药物;
血清稀释:将培养基中的老年血清替换为不含血清的基础培养液,模拟临床上的“治疗性血浆置换”[6]。
所有药物都有效果,但最显著的是“血清稀释+催产素”的组合。这个组合不仅将衰老标志p16的表达降至接近年轻水平,还恢复了脂肪细胞的胰岛素敏感性,改善了葡萄糖和脂质代谢功能。
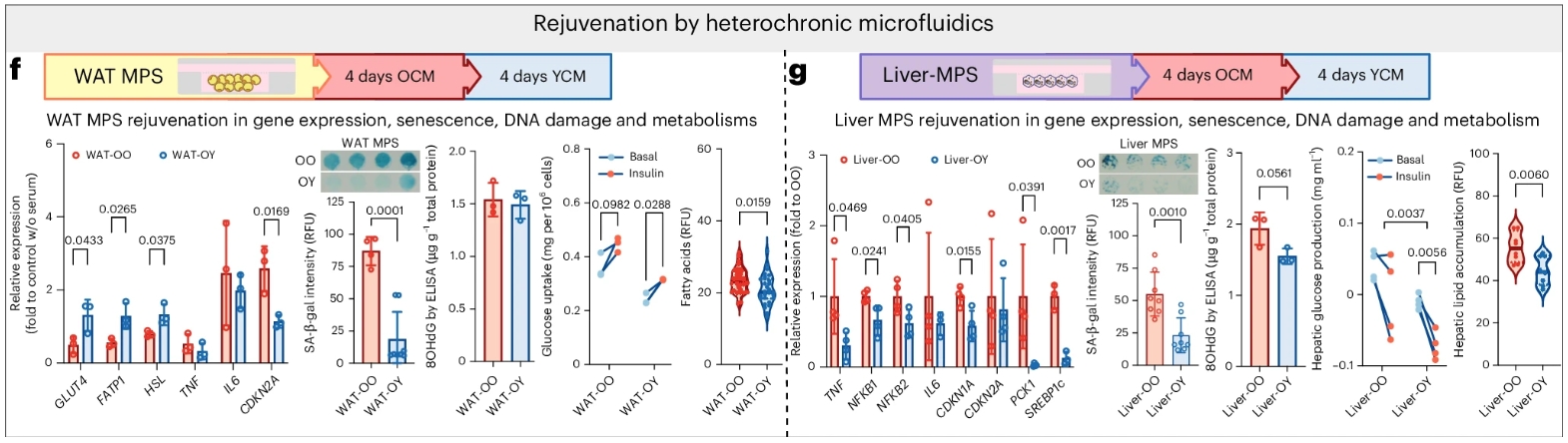
研究者还做了一个“血清切换”实验:先将芯片用老年血清处理4天,使其衰老,然后换成年轻血清再处理4天。结果发现,衰老的细胞可以部分逆转:炎症水平下降,代谢功能改善。这说明,人类组织的衰老并非不可逆,改变循环环境确实能够“拨动”生物学时钟。
最后,研究者通过RNAi技术专门敲低了衰老核心基因p16的表达。结果显示,即使不更换血清,仅阻断p16也能显著减轻衰老表型,印证了p16作为衰老“开关”的关键作用。
这项研究意味着什么?
从科学层面看,这项研究的核心价值在于提供了一个高临床相关性、快速、可重复的人类衰老研究平台。过去研究衰老,要么依赖动物模型(其结果未必适用于人类),要么耗费数十年进行人群队列研究。而这个芯片系统仅需4天就能模拟人类数十年的衰老过程,可以在数周内完成对一种药物的抗衰老效果评估。
另外,研究中揭示的几个现象尤其值得关注:
脂肪衰老会“传染”肝脏;
衰老具有“记忆性”——即使撤除老年血清,已经衰老的细胞仍会持续影响下游器官;
性别差异——即使细胞来自男性,用男性或女性的血清处理,芯片的衰老反应也截然不同。
总的来说,未来的抗衰老策略可能需要考虑性别因素,且单纯清除衰老细胞或许不够,还需要干预组织间的信号传递。
那对我们生活有什么用?
首先,“老”不只是年龄的增长,更是体内环境的变化。保持年轻态的血液环境,可能比单纯计算年龄更重要。

其次,脂肪组织并非只是能量仓库,它会分泌大量因子影响其他器官。控制体重、减少内脏脂肪,不只为身材,更是为了阻断脂肪向肝脏“传递衰老信号”。
最后,研究中效果最显著的干预手段之一是血清稀释,这对应到临床上已经在探索的“治疗性血浆置换”[6]。当然,这离普通人的日常保健还有很大距离,但指明了一个方向:清除血液中累积的有害因子,可能是未来延缓衰老的重要策略之一。
需要提醒的是,芯片上4天诱导的衰老,能否完全模拟数十年自然衰老的全部复杂性,仍有待更多验证。但对我们而言,健康饮食、规律运动等能帮助维持良好血液状态的生活方式,其价值可能比想象中的更大。
参考资料:
[1] Conboy, I. M., et al. (2005). Rejuvenation of aged progenitor cells by exposure to a young systemic environment. Nature, 433(7027), 760-764.
[2] Qi, L., et al. (2026). Human microphysiological systems of aging recreate the in vivo process expediting evaluation of anti-geronic strategies. Nature Biomedical Engineering.
[3] Wang, B., et al. (2024). The senescence-associated secretory phenotype and its physiological and pathological implications. Nature Reviews Molecular Cell Biology, 25(12), 958-978.
[4] The GTEx Consortium. (2013). The Genotype-Tissue Expression (GTEx) project. Nature Genetics, 45(6), 580-585.
[5] Li, E., et al. (2024). Control of lipolysis by a population of oxytocinergic sympathetic neurons. Nature, 625(7993), 175-180.
[6] Fuentealba, M., et al. (2025). Multi-omics analysis reveals biomarkers that contribute to biological age rejuvenation in response to single-blinded randomized placebo-controlled therapeutic plasma exchange. Aging Cell, 24(2), e70103.
[7] Zhang B, Lee DE, Trapp A, et al. Multi-omic rejuvenation and lifespan extension on exposure to youthful circulation. Nature Aging. 2023;3(8):948-964. doi:10.1038/s43587-023-00451-9
