“饿一饿,活得久”——这句话你八成在养生文章里见过。从线虫、果蝇到小鼠和猴子,把饭量减个两三成就延寿一小截,听起来像是进化的铁律。但你有没有好奇过:少吃两口饭,究竟是怎么在分子层面“骗”过衰老时钟的? 4月13日,美国耶鲁医学院的研究团队在《自然·衰老》上发表了一篇研究,首次从人类蛋白质组层面揭开了这个谜底。他们用了两年时间跟踪了42位每天只吃“八分饱”的健康中年人,在血浆里找到了一个很有意思的线索[1]。 早在1935年,美国康奈尔大学的克莱夫·麦凯(Clive McCay)团队就首次用大鼠证实:在保证营养的前提下减少热量摄入,确实能显著延长动物的寿命[5]。此后近百年,热量限制(Caloric Restriction,简称CR)在酵母、线虫、果蝇到小鼠、大鼠和猴子中被反复验证,成为衰老干预领域公认的非药物干预“金标准”。 但过去这些结论大多来自动物实验,对人类有没有同样的效果呢?2018年启动的CALERIE-II临床试验给出了答案——这是首个在健康非肥胖人群中开展的、为期两年的热量限制研究。参与者平均减少了约14%的热量摄入,差不多就是“吃八分饱”。两年后,这批人的胸腺功能增强、代谢指标改善、炎症水平降低[2,3]。简单说,身体的“生物年龄”确实变年轻了。 那么下一个问题来了:热量限制到底是通过什么机制做到这些的? 在新研究中,研究者对42位CALERIE-II参与者的血浆进行了高通量蛋白质组学分析,一口气检测了7000多种蛋白质。结果发现,热量限制后变化最显著的,是一个叫做“补体系统”的免疫通路。 补体系统是什么?通俗来讲,它是我们身体里的一支免疫部队,包含超50种蛋白质,其中的C3蛋白就像一个警报器。年轻时,补体系统只在感染或受伤时才会拉响警报(产生C3a),召集部队清理问题。 但人老了以后,这个警报器会变得过于灵敏,在没有真正威胁时也会持续发出微弱警报,导致身体一直处于“慢性低度炎症”状态,即衰老相关疾病的核心驱动力之一。因此,在老年人身上,C3和C3a水平会显著升高;甚至有研究发现,百岁老人体内C3水平越低,长寿概率越高,这是因为他们的免疫系统机能更健康,不会过度活跃地制造炎症,从而能抵御更多疾病[4]。 研究数据显示,两年热量限制后,参与者血浆中多条补体通路被显著抑制,尤其是C3a的水平大幅下降。最关键的一点是:这种下降与体重减轻无关,也就是说,即便你瘦得不多,只要坚持少吃,C3a依然会降低。 此外,研究人员利用“器官年龄”模型分析还发现,热量限制主要延缓了脂肪组织的蛋白质组衰老时钟,对其他器官影响不大。换句话说,内脏脂肪是热量限制发挥衰老干预作用的主要场所。 那么,血液里升高的C3a到底从哪来? 过去学界普遍认为肝脏是C3的主要合成部位,但这篇研究颠覆了这一认知。通过对比年轻和老年小鼠的多种组织,研究者发现:衰老带来的C3a升高,源头不在肝脏,而在内脏脂肪。实验数据显示,内脏脂肪中C3裂解产物的水平随年龄大幅增加,而肝脏中反而变化不大。 单细胞测序进一步锁定了罪魁祸首——内脏脂肪中的一种特定巨噬细胞亚群,被称为年龄相关巨噬细胞。这群细胞在老年小鼠的内脏脂肪中大量扩增,但有意思的是,它们并不表达p16和p21这些经典的“细胞衰老”标志物。也就是说,它们不是那些已经“死气沉沉”的衰老细胞,而是住在大肚腩里的一群“不衰老但就爱搞事”的邻居。 这群“坏邻居”通过一条“C3a-C3AR1-ERK”自分泌信号通路,持续自我激活,源源不断地释放促炎因子——IL-1β和IL-6等炎症因子随之升高,把整个脂肪组织变成了一座日夜冒烟的“炎症工厂”。这也解释了为什么肚子大的人往往炎症水平更高、老得更快,因为内脏脂肪不只是储存能量的仓库,更可能是驱动全身衰老的炎症策源地。 既然找到了肇事者,下一步就是验证能不能把它“关掉”。研究人员给20个月大的老年小鼠(相当于人类60岁左右)的内脏脂肪直接注射了C3a特异性中和抗体。结果相当干脆:短短3天后,血清中的关键炎症指标IL-1β和MCP-1显著下降;脂肪组织内的免疫环境也明显改善,促炎细胞减少,抗炎细胞增加。 更令人信服的是交叉验证。研究者还检测了另外两种已知能延长寿命的基因改造小鼠模型:FGF21过表达小鼠和PLA2G7缺失小鼠。结果表明,在这两种长寿模型中,C3a的水平同样显著低于同龄对照组。早在2022年就有研究发现,CALERIE-II参与者的PLA2G7基因表达下降,而该基因在小鼠中被敲除后可以部分模拟热量限制的抗炎效果。 这意味着:热量限制、FGF21过表达、PLA2G7缺失三种不同的长寿干预手段,最终都指向了同一个分子节点——C3a降低。就好像不同路径上的人,在同一个交叉路口汇合了。 冷静来看,补体系统是免疫防线的重要组成部分,长期完全关闭无疑会增加感染风险。不过论文也给这个矛盾留了一个出口:也许我们不必把补体彻底“关掉”,只要把“老年的过度激活”降回健康的基线水平就够了。而这个目标,离临床应用可能并不遥远。 对于我们普通人来说,哪怕只是每顿饭少吃几口,坚持下来就能在分子层面降低你的“炎症年龄”。当然,少吃不是“饿肚子”,而是要在保证营养均衡的前提下适度减少,绝不是节食或营养不良。其实,与其纠结每顿饭吃七分饱还是九分饱,身体里还有没有“慢性炎症”这个指标,可能才是更值得操心的事。 总之,“少吃两口饭”的衰老干预效果,未必是进化的铁律,它背后有一整套从脂肪、巨噬细胞到补体系统的连锁反应。也许在不远的将来,这套机制能被复制成一种更易操作的策略,不用饿肚子也能关掉那盏持续燃烧的“衰老炎症之火”。
热量限制——抗衰老界的“金标准”

补体系统——从“警报”变成“误报”
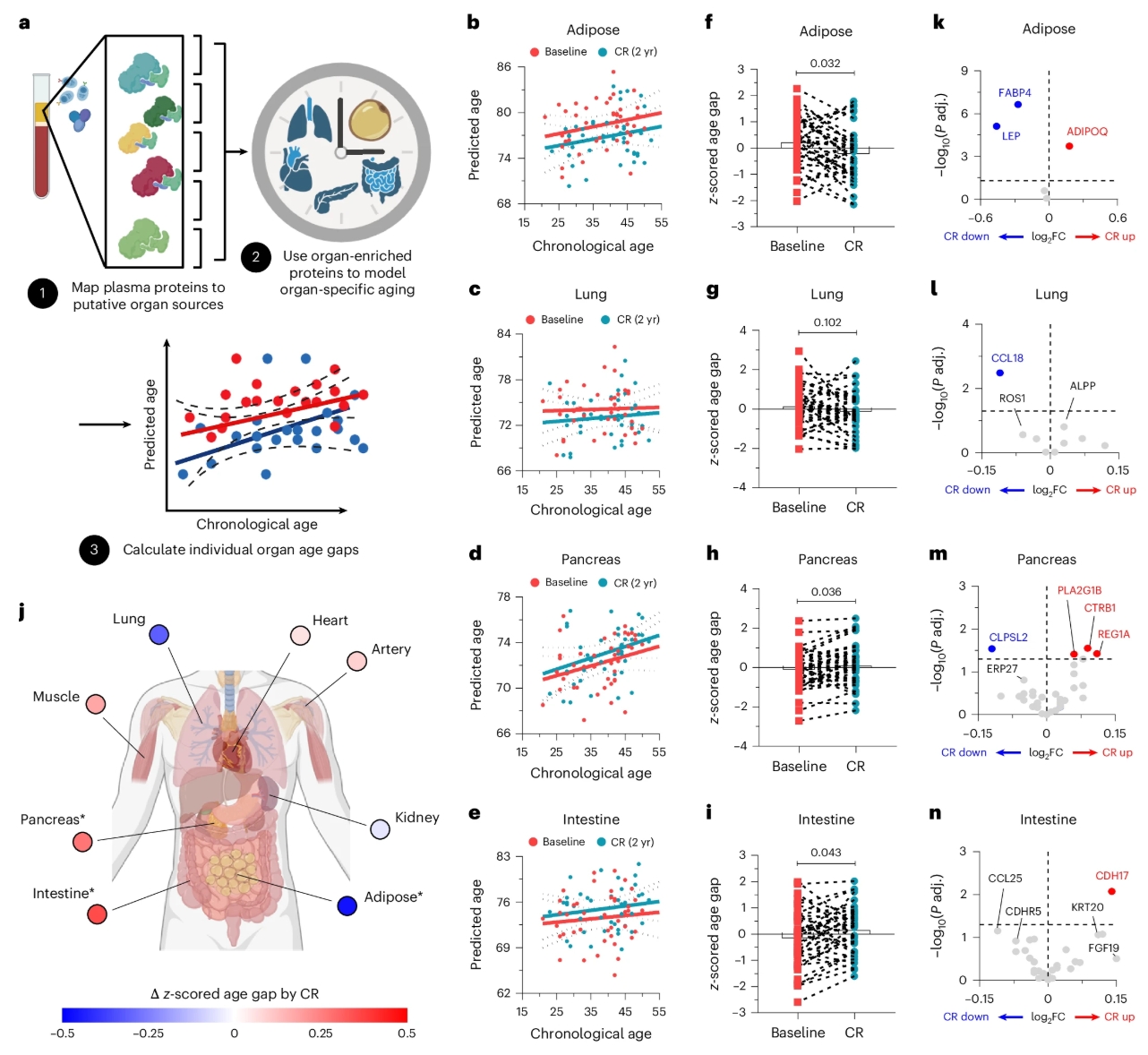
脂肪里的“坏邻居”——年龄相关巨噬细胞
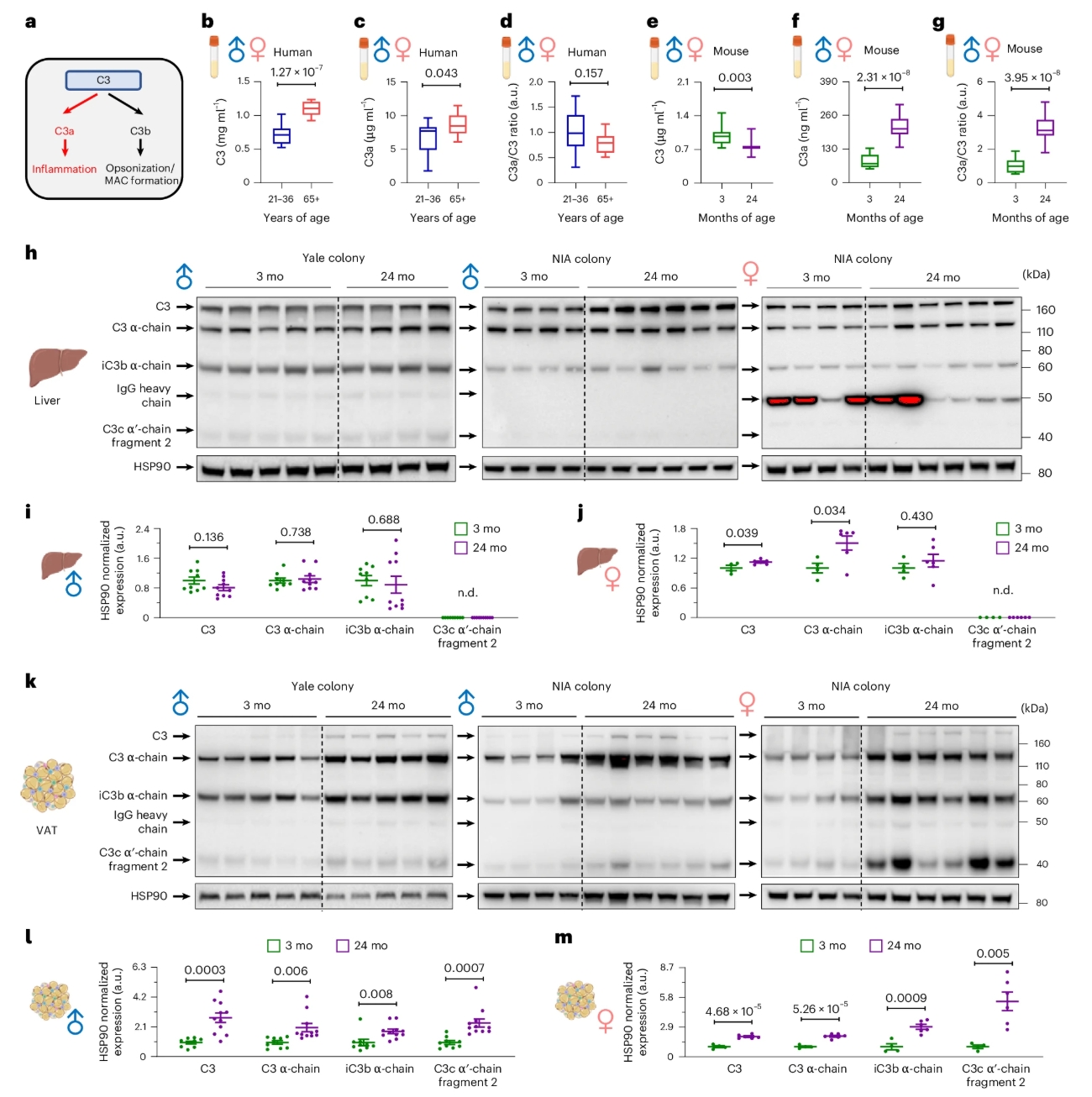
如果把炎症开关关掉
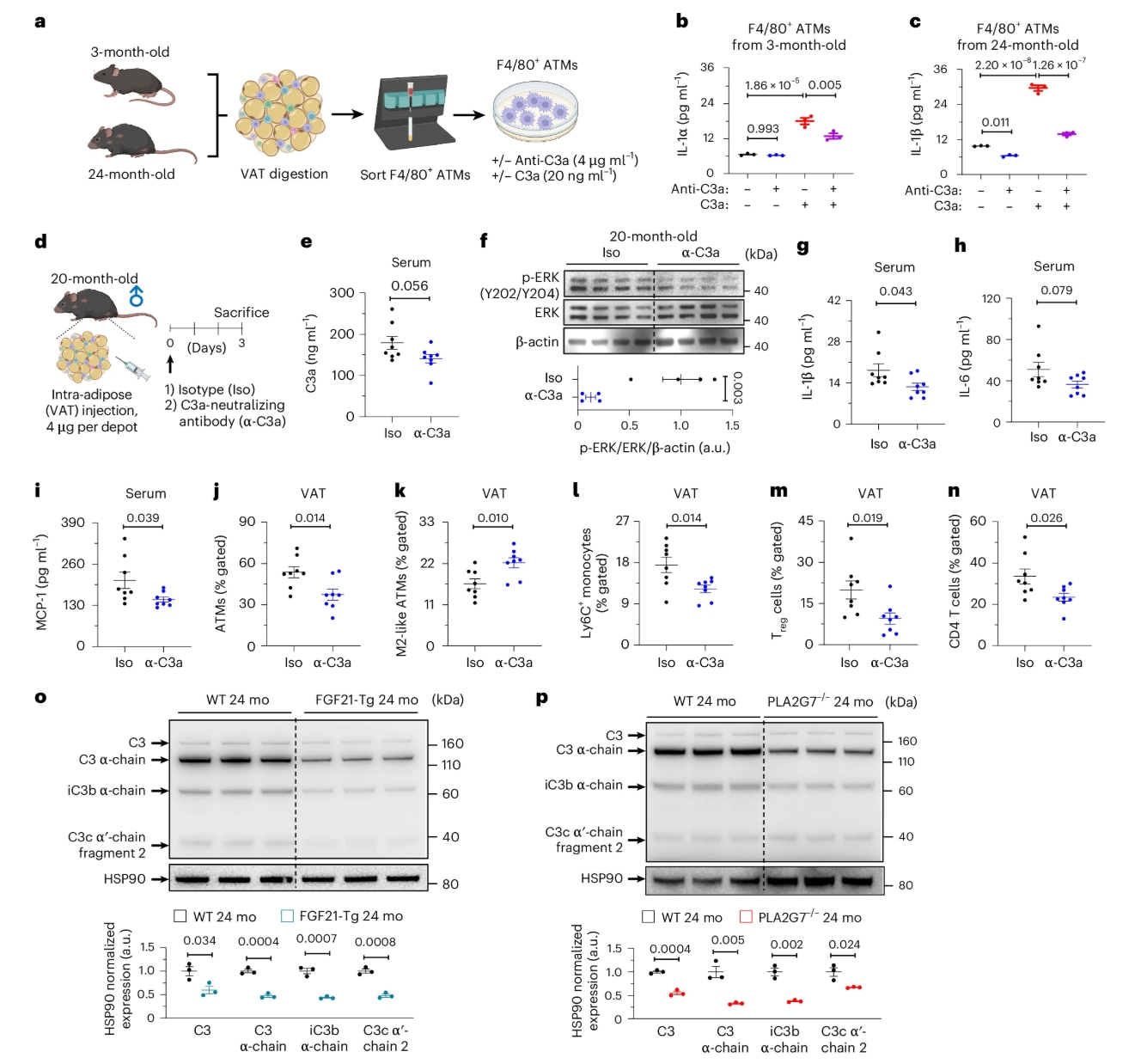
我们离“吞一颗药=延缓衰老”还有多远?

参考资料:
[1] Mishra M, Kim HH, Youm YH, et al. Exoproteome of calorie-restricted humans identifies complement deactivation as an immunometabolic checkpoint reducing inflammaging. Nature Aging. Published online August 6, 2025. doi:10.1038/s43587-026-01107-0
[2] Spadaro O, Youm Y, Shchukina I, et al. Caloric restriction in humans reveals immunometabolic regulators of health span. Science. 2022;375(6581):671-677. doi:10.1126/science.abg7292
[3] Ryu S, Sidorov S, Ravussin E, et al. The matricellular protein SPARC induces inflammatory interferon-response in macrophages during aging. Immunity. 2022;55(9):1609-1626.e7. doi:10.1016/j.immuni.2022.07.007
[4] Fu S, Li Y, Zhang F, et al. Centenarian longevity is positively correlated with IgE levels but negatively correlated with C3/C4 levels, abdominal obesity and metabolic syndrome. Cellular and Molecular Immunology. 2020;17(11):1196-1197. doi:10.1038/s41423-020-0386-y
[5] McCay CM, Crowell MF, Maynard LA. The effect of retarded growth upon the length of life span and upon the ultimate body size. Journal of Nutrition. 1935;10(1):63-79. doi:10.1093/jn/10.1.63
