人一旦上了岁数,不是心脏先出问题,就是最先感到记忆力下降,还有的人则是关节率先发出警报。这确实符合近几年的相关研究——不同器官的衰老速度可能不尽相同。

然而,今年2月美国洛克菲勒大学发表于国际顶刊《Science》的一项新研究发现,全身各个器官的衰老,其实是在同步进行的[1]。
器官衰老 “各自为政”?并不全对
我们先来回顾一下,为什么很多人会认为器官是“各老各的”?
2023年《Nature Medicine》上发表的一项研究,利用英国10万余人数据发现,肾脏可能比心脏老得更快,一个器官“超龄”还会增加其他系统的患病风险[2]。同年,另一国际顶刊《Nature》研究也指出,一位实际年龄50岁的人,心脏可能已经接近70岁的状态,而肝脏却还像个30岁的年轻人[3]。
2025年,《Cell》研究绘制了中国人群器官衰老时间表:30岁左右脂肪和肾上腺率先老化;35岁主动脉开始衰老,45岁时相关蛋白变化近40%;45至55岁为多器官加速衰老期,胰腺、脾脏尤为显著[4]。随后两个月,中国科学院昆明动物研究所牵头的团队围绕猕猴开展的研究同样显示,胸腺、脾脏、胃肠道、肾脏、卵巢等12个器官衰老速度较快,而大脑、肝脏、皮肤、肾上腺等11个器官衰老相对缓慢[5]。
所有这些研究都指向同一个结论:器官衰老确实有快有慢,各有各的“时间表”。
但问题来了,如果器官都在各自为政地老化,为什么人到了一定年纪,很多毛病会同时找上门?为什么50岁之后,高血压、糖尿病、骨关节炎、免疫功能下降几乎是结伴而来?
一张全身衰老的“染色质开关”地图
器官异步衰老并不意味着不同器官的衰老过程是彼此孤立的。上述由美国洛克菲勒大学研究团队发表在《Science》上的新研究就为这一观点提供了在单细胞层面的直接证据。新研究具体是怎么做的呢?
研究者使用了一种优化的单细胞染色质可及性测序技术——EasySci-ATAC。简单来说,这一技术可以检测基因组中哪些区域是“开放”的(即可以被转录因子结合、激活基因表达),哪些是“关闭”的。这种开放与关闭的状态,就是染色质的“开关”。
研究的规模相当大:覆盖21种小鼠组织(脂肪、肌肉、肾脏、肺、心脏、肠道等,不含大脑),三个年龄组(1个月、5个月、21个月),雌雄各半。共分析了超千个细胞核,最终鉴定出536种器官特异性主细胞类型、1828种更精细的细胞亚型,以及约134万个顺式调控元件。
这是第一次在全身、单细胞、表观遗传层面系统性地观察衰老。
衰老具有 “全身协同性”,但因性别不同
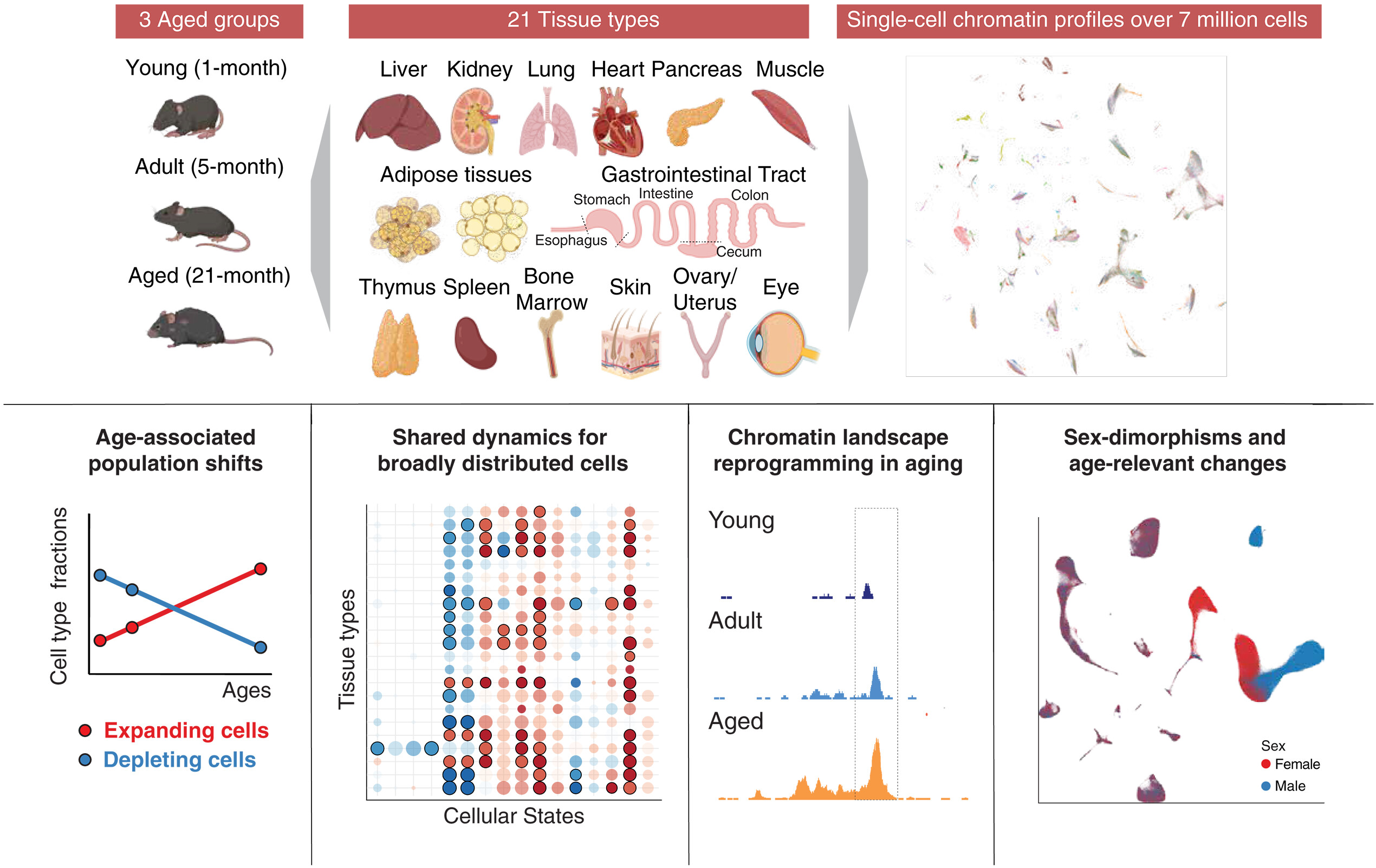
结果让研究者自己都有些意外:虽然不同器官的衰老速度不同,但当他们仔细分析单个细胞的状态变化时,发现大量衰老相关的变化在不同器官的细胞中竟然是同步发生的。具体来说,有以下几个核心结果:
免疫细胞:一边扩张,一边耗竭
衰老过程中,约四分之一的细胞类型出现显著数量变化。在免疫系统里,浆细胞、巨噬细胞等在多个器官中同时增加;研究鉴定出67种免疫亚型,其中多类T细胞和B细胞在不同器官里同步增多。
同时,初始CD4 T细胞在10个器官里减少,初始CD8 T细胞在5个器官里减少,骨髓中的B细胞祖细胞也普遍下降。这些是对抗新感染的关键储备,它们的同步减少解释了老年人为何更易感染。
非免疫细胞也存在跨器官同步
一些不循环的细胞同样表现出协同性。一种静脉内皮细胞在肌肉、脂肪、卵巢/子宫中同步减少;另一种炎症性成纤维细胞在胃、盲肠、食道、脂肪中同步增加,且只发生在雄性身上。
肾脏中还发现三种反应性上皮细胞,在老年雌性中共同扩张,都高表达炎症相关基因。这种特征并非肾脏独有,其他器官的衰老细胞中也能看到。
表观遗传层面:统一的“炎症开关”
超过27万个染色质区域随年龄改变,其中803个区域在至少10种细胞类型中一致变化。Nr3c2(与血压、炎症相关)的启动子在63种细胞类型中更开放;促炎因子Il7的启动子在26种细胞类型中开放增加。而干细胞相关基因Sox4和Sox11的启动子分别在25种和19种细胞类型中关闭。
衰老中更开放的区域富集炎症转录因子(AP-1、IRF、NF-κB)的结合位点;关闭的区域富集干细胞维持因子。这意味着衰老在表观遗传层面是从“维持稳态”向“促炎状态”的全身性转变。此外,原本被压制的“垃圾DNA”(LINE/LTR转座子)在衰老细胞中变得开放,导致基因组不稳定。
性别差异:男女衰老“剧本”不同
约40%的变化存在性别依赖。雌性免疫扩张更强(53 vs 31种亚型),可能解释女性自身免疫病更高发。但雄性在胃肠道有更多扩张的免疫亚型。分子层面,雌性有19.5万个、雄性有14万个独特的染色质变化。例如,衰老雌鼠肝细胞中细胞外基质重塑相关基因更开放,雄鼠肾细胞中程序性细胞死亡相关基因更开放。
新旧观点并不矛盾,而是一种互补
看到这里你可能有点困惑:前面说器官各有各的衰老时间,现在又说全身同步衰老,到底哪个对?
实际上,器官各有各的衰老节奏,但衰老又确实存在跨器官的协同性[6]。这两个看似矛盾的结论,其实可以在不同尺度上统一起来:
器官功能衰退看的是“宏观速度”,比如心脏泵血能力、肾脏滤过率、肌肉力量等,这些指标的下降速度确实因器官而异;
细胞群体的变化看的是“微观同步”,包括特定类型的免疫细胞、内皮细胞、成纤维细胞,它们的扩增或耗竭则是全身性的。
普通人能做什么?
这项研究虽然基于小鼠,但它揭示的机制——系统性炎症、染色质调控失灵、免疫细胞失衡——在人类身上同样存在,并且指向了几个有科学依据的日常干预方向。
抗炎是主线
研究核心发现之一是:衰老在表观遗传层面表现为炎症通路的全面激活。反过来看,抑制慢性低度炎症可能是延缓衰老的关键。

有充分证据支持的抗炎策略包括:地中海饮食(多蔬菜、水果、全谷物、橄榄油、鱼类,少红肉和加工食品);有氧与抗阻结合的运动;充足睡眠和压力管理。2025年的一项社论指出,低炎症饮食与减缓生物学衰老相关,可以抵消体力活动不足的有害影响[7]。
保护功能细胞
研究中发现肾脏足细胞、肌肉卫星细胞等在衰老中显著减少。虽然无法直接“阻止”这种减少,但可以通过减轻对应器官的代谢负担来延缓:控制血压血糖保护肾脏;规律抗阻训练维持肌肉量;避免长期高脂高糖饮食减轻代谢应激。
恢复免疫平衡,而非“增强免疫力”
衰老的免疫系统不是单纯“变弱”,而是变得“失衡”:炎症效应细胞(浆细胞、巨噬细胞)过度活跃,而应对新病原体的初始T细胞和B细胞祖细胞储备不足。
可行的策略包括:保证优质蛋白质摄入;适量补充维生素D;避免长期慢性压力(皮质醇升高会抑制淋巴细胞生成);按时接种流感疫苗、肺炎疫苗、带状疱疹疫苗等[8]。

热量限制,但不盲目节食
热量限制被证明可部分恢复干细胞功能、减轻表观遗传年龄。但老年人需保证足够蛋白质摄入以维持肌肉量和免疫功能。二甲双胍、雷帕霉素、希诺裂等药物仍处于研究阶段,不宜自行服用。
器官各老各的,但细胞却在同步“发炎”。这意味着单一靶点的抗衰老药很难奏效,延缓衰老更需要系统性地干预。如果我们能从根源上控制慢性炎症,也许就能同时延缓多个器官的衰老。
参考资料:
[1] Lu Z, Zhang Z, Xu Z, Abdulraouf A, Zhou W, Cao J. Organism-wide cellular dynamics and epigenomic remodeling in mammalian aging. Science. 2026;391(6788):eadw6273. doi:10.1126/science.adw6273
[2] Tian YE, Cropley V, Maier AB, Lautenschlager NT, Breakspear M, Zalesky A. Heterogeneous aging across multiple organ systems and prediction of chronic disease and mortality. Nature Medicine. 2023;29(5):1221-1231. doi:10.1038/s41591-023-02296-6
[3] Oh HSH, Rutledge J, Nachun D, et al. Organ aging signatures in the plasma proteome track health and disease. Nature. 2023;624(7990):164-172. doi:10.1038/s41586-023-06802-1
[4] Ding Y, Zuo Y, Zhang B, et al. Comprehensive human proteome profiles across a 50-year lifespan reveal aging trajectories and signatures. Cell. 2025;188(20):5763-5784.e26. doi:10.1016/j.cell.2025.06.047
[5] Li GH, Zhu XQ, Xiao FH, et al. A multi-omics molecular landscape of 30 tissues in aging female rhesus macaques. Nature Methods. 2025;22(12):2658-2669. doi:10.1038/s41592-025-02912-y
[6] Rando TA, Wyss-Coray T. Asynchronous, contagious and digital aging. Nature Aging, 2021, 1: 29-35.
[7] Paoli A, Siow R, Moro T. Editorial: Spotlight on aging: role of exercise and nutrition in healthy longevity. Frontiers in Aging. 2025;6:1698219. doi:10.3389/fragi.2025.1698219
[8] Chen JB, Wang MC, Gong S, Li H. Toward precision longevity: aging interventions in the single-cell atlas era. Frontiers in Aging. 2025;6:1674112. doi:10.3389/fragi.2025.1674112
