当我们谈论记忆力下降时,通常首先想到的是大脑本身的问题。阿尔茨海默病、脑血管病变、神经元的自然衰老——这些确实是认知衰退的重要原因。
但3月11日发表于国际顶刊《自然》的一项研究提出了新观点,一个看似与大脑无关的领域———肠道微生物,可能对我们的认知功能有重要影响[1]。

新研究首次系统地描绘了一条从肠道细菌、免疫细胞到迷走神经,最终影响海马体功能的完整通路。美国Arc研究所和斯坦福大学的研究人员发现,随着年龄增长,一种特定肠道细菌的过度增殖会通过一系列连锁反应,削弱肠道向大脑传递信号的能力,进而影响记忆功能。
把老年小鼠的肠道菌群给年轻小鼠,会发生什么?
研究团队首先设计了一组简单的实验。他们将2个月大的年轻小鼠(相当于人类寿命不到20岁)与18个月大的老年小鼠(相当于人类寿命56岁)放在同一个笼子里饲养。一个月后,年轻小鼠的肠道菌群结构发生了变化,变得更接近老年小鼠。与此同时,这些年轻小鼠在新物体识别测试和迷宫测试中的表现显著下降。换句话说,它们的短期记忆和空间记忆都受到了损害。
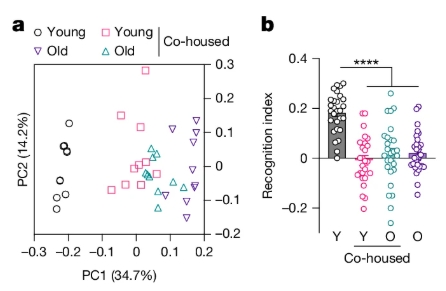
为了排除共同生活本身带来的社交因素影响,研究者又进行了另一组实验:将老年小鼠的粪便微生物移植给无菌饲养的年轻小鼠。结果竟然一致,接受了老年菌群的年轻小鼠也出现了记忆能力下降。相反,如果让年轻无菌小鼠与老年无菌小鼠同居(两者都没有肠道菌群),年轻小鼠的认知能力并未受损。这说明,导致认知功能下降的关键因素正是肠道菌群本身,而不是衰老带来的其他身体变化。
锁定“嫌疑菌”:Parabacteroides goldsteinii
有了明确的现象,下一步就是找出具体是哪一种或哪几种细菌在起作用。研究者对小鼠从断奶到死亡的全生命周期进行了纵向宏基因组测序,追踪菌群随年龄的变化,并设定了一个筛选标准:随年龄增长而丰度增加,并且能够通过同居或粪菌移植传递给年轻小鼠的细菌。
经过筛选,一种名为Parabacteroides goldsteinii(戈氏副拟杆菌)的肠道细菌成为首要候选对象。在老年小鼠的肠道中,这种细菌的丰度显著高于年轻小鼠,且能够通过同居或粪菌移植传递给年轻个体。
为了验证因果关系,研究者将P. goldsteinii单独定植到无菌小鼠或经过抗生素处理清除自身菌群的小鼠体内。结果证实,仅仅是这一种细菌的存在,就足以导致认知能力下降。相比之下,其他几种同样随年龄变化的细菌(如Alistipes或Lactobacillus)并未产生同样的效果。
细菌如何“隔空”影响大脑?
细菌本身不会直接进入大脑,应该是通过某些化学物质或代谢产物发挥影响。研究者从P. goldsteinii的培养液中提取了上清液(不含细菌,仅含其分泌的代谢物),喂给年轻小鼠。结果依然出现了认知障碍。
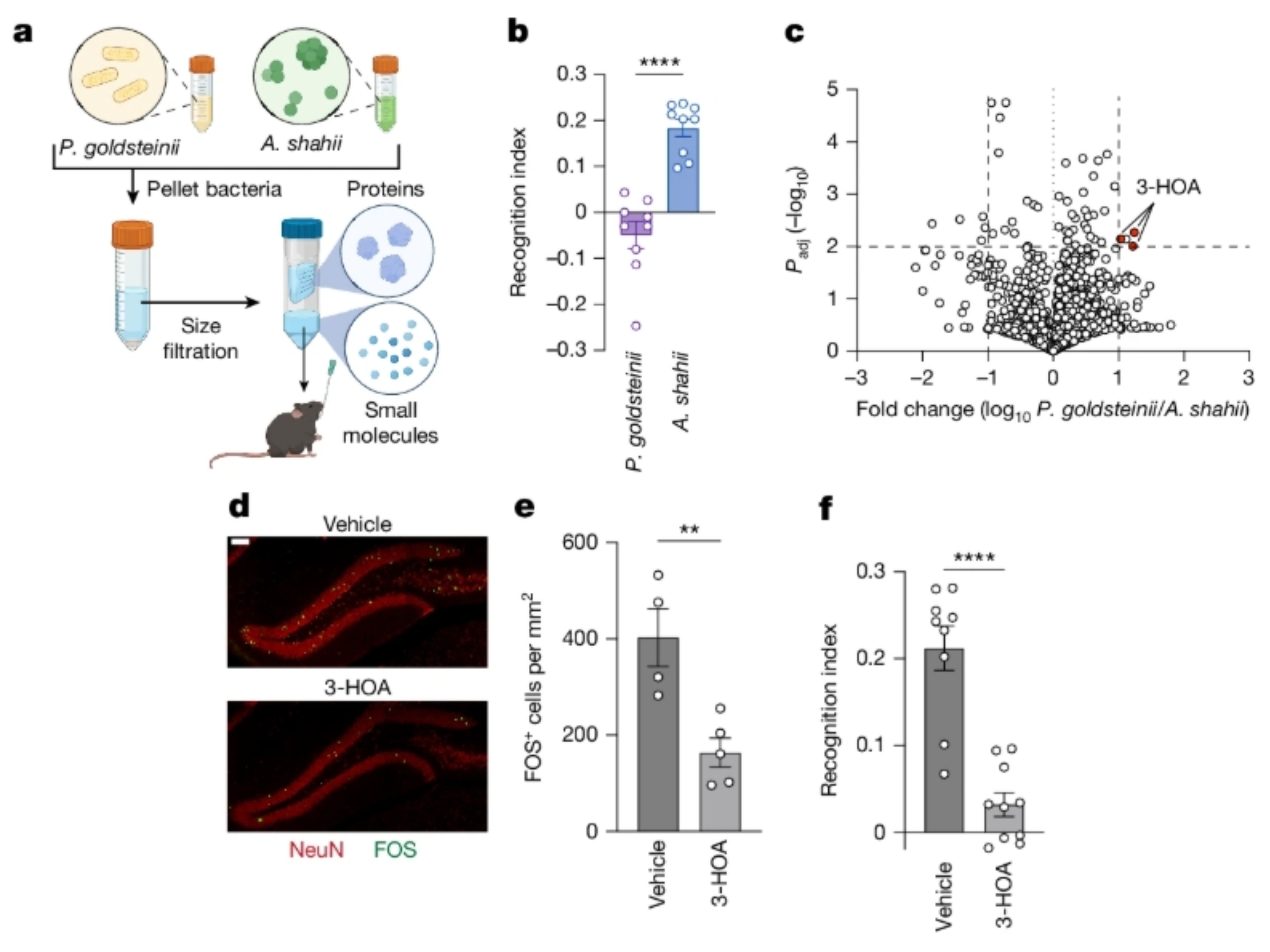
分析这些上清液中的成分,研究者发现:中链脂肪酸(MCFA)——特别是3-羟基辛酸(3-HOA)——在P. goldsteinii的培养液中显著富集,直接给小鼠口服3-HOA或癸酸(另一种中链脂肪酸)后,小鼠同样出现了记忆功能下降。
那么,这些脂肪酸究竟做了什么?研究者发现,它们激活了一种名为GPR84的受体,而这种受体几乎只在髓系免疫细胞(如巨噬细胞、单核细胞)上表达。GPR84被激活后,会促使这些免疫细胞释放两类关键的炎症因子:肿瘤坏死因子(TNF)和白细胞介素-1β(IL-1β),从而加速大脑衰老。
炎症因子如何切断肠-脑信号?
近年,市面上有很火的一种说法,叫“肠-脑轴”,其实是肠道和大脑之间的一条重要“热线”——迷走神经。迷走神经从脑干发出,延伸至腹腔,负责将肠道的感觉信号传递回大脑。研究者通过钙成像技术观察到,携带老年菌群的年轻小鼠,其迷走神经元对肠道营养刺激的反应明显减弱:无论是反应神经元的数量,还是单个神经元的反应强度,都低于对照组。
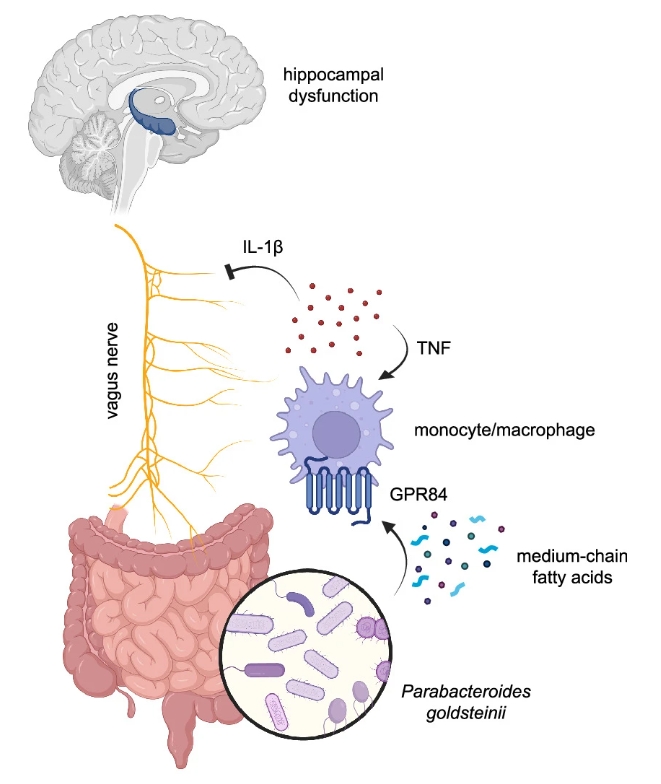
进一步实验显示,IL-1β可以直接作用于迷走神经元,削弱其功能。当研究者敲除了迷走神经元上的IL-1β受体后,中链脂肪酸不再能引起认知障碍。换句话说,免疫细胞释放的炎症因子攻击了迷走神经,导致肠道向大脑发送的信号减弱。
迷走神经功能受损的直接后果是大脑接收不到足够的“内感受信号”,即来自身体内部的感知信息。研究者检测了小鼠海马体(负责记忆形成的关键脑区)在接触新物体后的神经元激活情况。结果显示,无论是老年小鼠、与老年同居的年轻小鼠,还是P. goldsteinii定植的年轻小鼠,其海马体中被激活的神经元数量都显著减少。
能否逆转?——多项干预手段的验证
既然找到了这条通路,研究者自然要问:能不能通过干预来逆转认知衰退?结果还真可以!他们在实验中验证了多种策略:
第一种策略是直接激活迷走神经
研究者给老年小鼠注射了低剂量的TRPV1激动剂(可激活迷走神经),结果显示,老年小鼠的记忆功能恢复到了年轻小鼠的水平。胆囊收缩素(CCK)和GLP-1受体激动剂(如利拉鲁肽)这两种已知能刺激迷走神经的肠肽,同样起到了改善认知的效果。
第二种策略是阻断GPR84信号
使用GPR84抑制剂PBI-4050后,中链脂肪酸诱导的认知障碍被完全逆转。在GPR84基因敲除的小鼠中,中链脂肪酸也失去了致病作用。
第三种策略是清除外周髓系免疫细胞
研究者使用CSF1R抑制剂PLX-3397、氯膦酸脂质体(不进入大脑,仅清除外周吞噬细胞),或通过CCR2基因敲除(减少单核细胞向组织的浸润),均能阻断中链脂肪酸对认知的影响。
第四种策略是中和炎症因子
注射TNF或IL-1β的中和抗体,同样能够保护小鼠免受认知衰退的困扰。
最后,研究者还尝试了噬菌体疗法
特定噬菌体虽不能直接杀死P. goldsteinii,但能够改变其基因表达,减少肠道中中链脂肪酸的水平,从而改善老年小鼠的认知功能。
基于这项研究,生活中能做什么?
需要重点说明的是,这项研究目前仅在小鼠中完成,从实验室到人类应用还有很多复杂的步骤。但基于新研究揭示的机制,长寿之家changshou.com总结出以下可能有助于预防认知衰退的参考建议:
关注饮食中的脂肪酸结构
MCFA在椰子油、棕榈油中含量较高。虽然这些油脂被一些人宣传为“健康脂肪”,但本研究提示,长期过量摄入MCFA可能对认知产生负面影响。对于中老年人而言,平衡脂肪酸来源、避免单一油脂的大量摄入,是合理的预防思路。

增加膳食纤维,维持菌群多样性
富含纤维的食物(全谷物、豆类、蔬菜、水果)有助于抑制条件致病菌的过度生长,是维持肠道菌群健康多样性的基础。
通过生活方式增强迷走神经张力
生活中,深呼吸(尤其是缓慢的腹式呼吸)、冥想、冷暴露(如冷水洗脸)、适度有氧运动都被证实能提高迷走神经活性。
控制慢性炎症水平
研究表明,外周炎症因子是连接肠道菌群与迷走神经的桥梁。长期高糖、高精加工食品的饮食会促进低度炎症,而富含ω-3脂肪酸(深海鱼、亚麻籽)、多酚类物质(浆果、绿茶、黑巧克力)的饮食具有抗炎作用。
调整肠道菌群结构
增加有益菌可能有助于维护菌群平衡,比如鼠李糖乳杆菌、乳双歧杆菌、长双歧杆菌等,对认知功能和记忆力可能有显著改善[2,3]。不过,补充益生菌的具体菌株和剂量因人而异,建议在了解自身肠道状况后进行合理选择。

谨慎使用抗生素
非必要的抗生素使用会破坏菌群生态,可能为致病菌(如P. goldsteinii类)的过度增殖创造条件。在医生指导下合理使用抗生素,是保护肠道菌群的基本原则。
肠道与大脑之间的关系,远比我们想象的要复杂和重要。或许在未来,健康体检会包含肠道菌群的检测,预防认知衰退的干预措施也会从肠道入手。从当下看,维护肠道健康,或许也是让大脑保持年轻的一种方式。
参考资料:
[1]Cox TO, Devason AS, De Araujo A, et al. Intestinal interoceptive dysfunction drives age-associated cognitive decline. Nature. March 2026.
[2]Ruiz-Gonzalez C, Cardona D, Rueda-Ruzafa L, Rodriguez-Arrastia M, Ropero-Padilla C, Roman P. Cognitive and Emotional Effect of a Multi-species Probiotic Containing Lactobacillus rhamnosus and Bifidobacterium lactis in Healthy Older Adults: A Double‐Blind Randomized Placebo‐Controlled Crossover Trial. Probiotics and Antimicrobial Proteins. 2024;17(5):3525-3537.
[3]Da Costa MB, Borges CG, Tufik S, Antunes HKM. Effect of psychobiotic supplementation on cognitive function in the elderly: a randomized controlled pilot study. Medicine & Science in Sports & Exercise. 2024;56(10S):637.
