阿尔茨海默症(AD)被许多人称为“不可死的癌症”,它的可怕之处在于:它虽不会直接致命,却会以最残酷的方式摧毁患者的记忆、认知和生活能力。这对于患者本身、患者家属和整个社会都是个巨大的挑战。更残酷的是,阿尔茨海默症至今无药可医,这让无数家庭在绝望中挣扎。
但就在这个月初,暨南大学与奥斯陆大学合作在《科学·进展》(Science Advances)上发表的一项研究,为我们带来新的希望。研究人员发现——补充NAD+(烟酰胺腺嘌呤二核苷酸)能够逆转阿尔茨海默症的神经功能缺陷,并将模型生物寿命延长17%[1]。

而且,NAD+的作用方式也颠覆了传统认知:不是清除淀粉样斑块,也不是直接溶解Tau蛋白缠结,而是深入细胞核,修复基因表达的"剪接错误"——从根本上纠正致病过程。
阿尔茨海默症的新视角:RNA剪接出错
过去,我们对阿尔茨海默症的理解,大多聚焦于两种标志性的病理特征:大脑中β-淀粉样蛋白沉积形成的“斑块”,和Tau蛋白过度磷酸化形成的“神经纤维缠结”[2]。它们通常被视作摧毁神经元、导致记忆丧失的“元凶”。
但这项研究指出了一个更深层的根源——RNA的剪接异常。
科学家通过转基因手段制备了AD小鼠模型,以Tau蛋白过度磷酸化为病理特征,和健康野生型小鼠的海马体组织进行了RNA测序分析,结果发现:与野生型小鼠相比,AD小鼠海马体中下调的基因多与RNA剪接调控过程相关,这说明RNA剪接异常是AD小鼠病理特征的标志性表现。
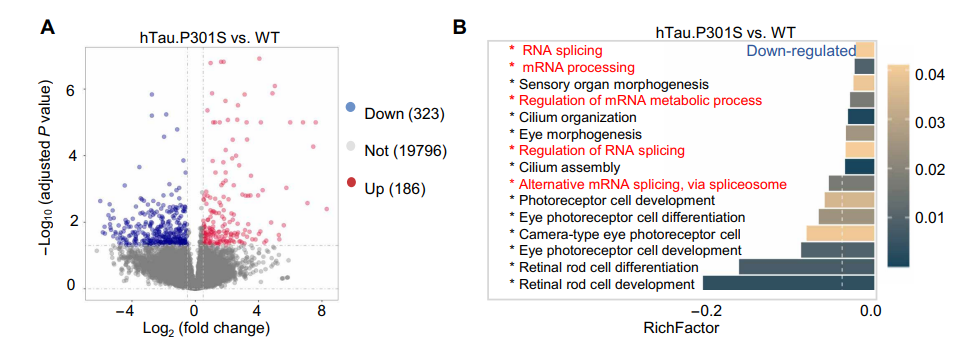
什么是“RNA剪接”?我们可以把RNA剪接想象成视频剪辑的过程。DNA由内含子与外显子组成,内含子就像“拍摄的废片”,在转录成mRNA之后要被剪掉;而外显子就像拼成“成片”的片段。
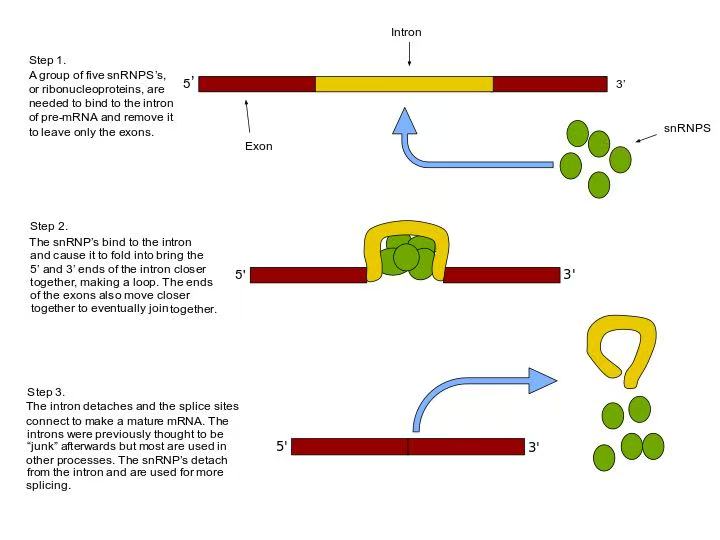
通过不同的剪辑方式,同一段基因可以“剪辑”出功能各异、甚至功能完全丧失的蛋白质版本。随着遗传、环境、年龄等因素的改变,RNA剪接过程可能出现异常,会导致细胞功能紊乱,进而引发疾病。
显然,研究人员认为在阿尔茨海默症小鼠的大脑中正是如此。
RNA的剪接错误,NAD+来修正
NAD+(烟酰胺腺嘌呤二核苷酸)是细胞内一种非常重要的辅酶,它参与能量代谢、DNA修复、细胞衰老等多个生物过程。人体内的NAD+水平随着年龄增长逐渐下降,与衰老、代谢疾病以及神经退行性疾病的发生密切相关。
近年来诸多研究发现,在哺乳动物中补充NAD+的前体物质(如烟酰胺核苷NR/烟酰胺单核苷酸NMN)展示出了对AD不同程度的改善功能[3-6],还有多项人体临床试验正在进行中。
同样,该研究中也通过RNA测序发现,给AD小鼠喂养NR,与对照组相比,小鼠的海马体多维RNA剪接有所改善。
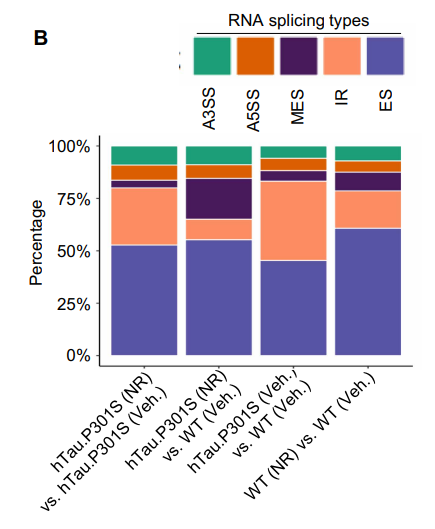
并且,研究者在多种AD模型中,包括线虫、小鼠和人类细胞,发现使用NAD+前体NMN/NR喂养会显著影响EVA1C这一基因的表达。EVA1C是一种免疫球蛋白超家族蛋白,在神经元发育和功能中起重要作用。因此研究者推测:NAD+是通过调控EVA1C这一基因的表达和剪接来影响神经元功能的。
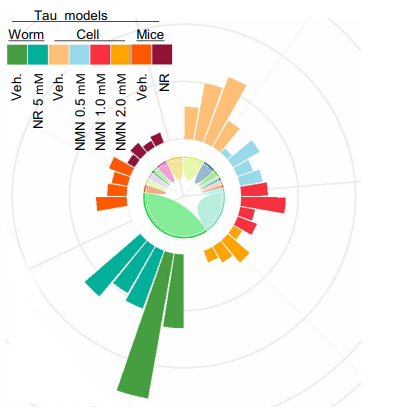
NAD+——延长寿命,提升记忆力
研究仅停留在基因层面显然是远远不够的,研究团队还做了行为观察实验,发现在不同的模式动物中,NAD+不仅能延长AD线虫的寿命,还能恢复AD小鼠的记忆缺失。
延长寿命
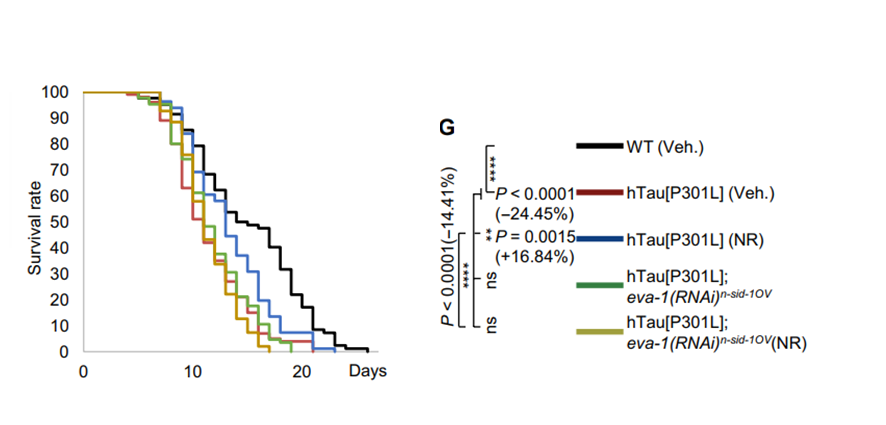
研究人员发现,2 mM的NR喂养,可以将AD线虫的寿命延长16.84%(下图中蓝色曲线和红色曲线对比)。但是如果把线虫中与人EVA1C同源基因eva-1敲除,并未观察到NR对于寿命的延长作用(深绿和浅绿曲线),这说明NR起作用是依赖EVA1C基因的。
行为改善:NAD+让AD小鼠记忆“重获新生”
为了验证这一猜想,研究人员在AD小鼠海马体中注射两种腺病毒,分别过表达和敲低EVA1C。
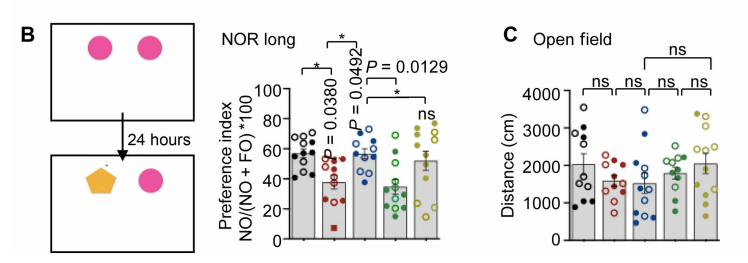
接着在行为学实验中,研究人员发现:接受NAD+前体处理的AD模型小鼠,在“新物体识别”测试中表现出显著更好的记忆能力。意料之中,如果EVA1C被敲除,NAD+就无法发挥作用。
这说明, NAD+ → EVA1C → 记忆改善是一条清晰的信号通路。NAD+必须通过EVA1C才能修复神经元的记忆丧失。
NAD+增强神经保护——人类同样适用
研究还扩展到人类样本的分析。研究者发现,在阿尔茨海默症患者的大脑中,EVA1C的表达显著下降,尤其在海马体和内嗅皮层这些AD最早受损的脑区。此外,EVA1C的表达水平与患者的临床病理分期、认知评分等指标密切相关,这一发现进一步验证了EVA1C在AD中的关键作用。
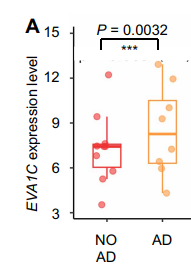
阿尔茨海默病患者与对照组(无AD)间EVA1C的差异表达(参考资料[1])
这些数据为我们提供了强有力的证据,表明NAD+通过调控EVA1C修复RNA剪接异常,可能成为治疗阿尔茨海默症的一个潜在新途径。
保护大脑,我们还能做些什么?
但是神经系统是极其复杂的,大脑衰老也不是单一通路作用的结果,想要真正逆转AD没有那么容易,未来最有效的干预手段或许是“多通路协同干预”——在维持NAD+水平的基础上,结合其他经科学验证的方法,才能达到更为理想的效果。
那我们还可以做些什么呢?
除了长寿之家Changshou.com之前多次提及的保持积极社交、规律运动和认知训练外,一些具有潜在神经活性的补充剂也显示出应用前景,例如:
1、α-硫辛酸:
α-硫辛酸是一种强抗氧化剂,具有一定的神经保护作用。一项为临床试验结果显示,多发性硬化症(MS)患者坚持服用α-硫辛酸2年后,脑容量的减少幅度显著小于预期[7]。
2、茶氨酸:
茶氨酸具有镇静作用,有临床试验研究表明,茶氨酸可以通过缓解压力、改善睡眠来提升受试者的认知功能[8]。
3、甜菜碱:
甜菜碱是一种生物碱,是体内一碳代谢的重要甲基供体,被报道可以降低阿尔茨海默症患者的Tau 蛋白磷酸化水平,并且改善认知功能,同时也能预防心血管疾病风险[9]。
4、槲皮素:
作为希诺裂(衰老细胞清除剂/Senolytics)的一种,经典的达沙替尼+槲皮素组合被证明可以改善患者的数学认知水平[10]。

在中国,每7秒钟就会增加一位阿尔茨海默症患者,全球范围内,阿尔茨海默症的蔓延速度同样惊人。根据世界卫生组织的数据,全球有超过5500万名痴呆症患者,预计到2050年,这个数字还会翻一倍。
自1906年阿尔茨海默医生首次描述这一疾病至今,人类与之抗争已逾百年。无数科学家在漫长的探索中不断试错,终于在这项最新的研究中,我们看到了NAD+逆转阿尔茨海默症的希望。
我们期待看到那一刻:患病的母亲可以重新叫出儿子的名字,重拾过往美好的记忆碎片,健康地度过余年……相信那一天,正在越来越近。
参考资料:
[1] Ai, R. et al. NAD + reverses Alzheimer’s neurological deficits via regulating differential alternative RNA splicing of EVA1C. Science Advances 11, eady9811 (2025).
[2] Llibre-Guerra, J. J. et al. Towards pharmacological prevention of Alzheimer disease. Nature Reviews Neurology (2025) doi:10.1038/s41582-025-01154-y.
[3] Lautrup S., Sinclair D. A., Mattson M. P., Fang E. F., NAD+ in brain aging and neurodegenerative disorders. Cell Metab. 30, 630–655 (2019).
[4] Dong Y., Brewer G. J., Global metabolic shifts in age and Alzheimer’s disease mouse brains pivot at NAD+/NADH redox sites. J. Alzheimer’s Dis. 71, 119–140 (2019).
[5] Hou Y., Lautrup S., Cordonnier S., Wang Y., Croteau D. L., Zavala E., Zhang Y., Moritoh K., O’Connell J. F., Baptiste B. A., Stevnsner T. V., Mattson M. P., Bohr V. A., NAD+ supplementation normalizes key Alzheimer’s features and DNA damage responses in a new AD mouse model with introduced DNA repair deficiency. Proc. Natl. Acad. Sci. U.S.A. 115, E1876–E1885 (2018).
[6] Liu D., Pitta M., Jiang H., Lee J. H., Zhang G., Chen X., Kawamoto E. M., Mattson M. P., Nicotinamide forestalls pathology and cognitive decline in Alzheimer mice: Evidence for improved neuronal bioenergetics and autophagy procession. Neurobiol. Aging 34, 1564–1580 (2013).
[7] Spain, R. et al. Lipoic acid in secondary progressive MS. Neurology Neuroimmunology & Neuroinflammation 4, (2017).
[8] Hidese, S. et al. Effects of L-Theanine Administration on Stress-Related Symptoms and Cognitive Functions in healthy adults: a randomized controlled trial. Nutrients 11, 2362 (2019).
[9] Sun, J., Wen, S., Zhou, J., Ding, S., 2016. Association between malnutrition and hyperhomocysteine in Alzheimer’s disease patients and diet intervention of betaine. J. Clin. Lab. Anal. 31, e22090.
[10] Millar, C. L. et al. A pilot study of senolytics to improve cognition and mobility in older adults at risk for Alzheimer’s disease. EBioMedicine 113, 105612 (2025).
