“虚弱”在日常语言里是一个模糊的词,但“衰老性虚弱”(frailty)已被世界卫生组织(WHO)将正式纳入疾病分类目录,承认它是一种可识别、可干预的临床综合征。这意味着,随着年龄增长而变得体力不支、行动迟缓,已经不再只是“老了就这样”的宿命,而是一个可以被医学认真对待的状态。
但在过去,针对这一综合征,临床上几乎没有经过严格验证的有效疗法。

好消息是,近期发表于《Cell Stem Cell》的一项随机临床试验给虚弱老人带来了希望:向体内输注来自年轻健康捐献者骨髓的异体间充质干细胞(MSCs),可以显著改善甚至逆转虚弱老人的身体功能。
这项研究的背后,是一个已经走过十余年的临床开发历程,以及一个关于衰老生物学的更大问题:人体的退化是否可以被“重新校准”?
什么是衰老性虚弱,为什么它值得严肃对待
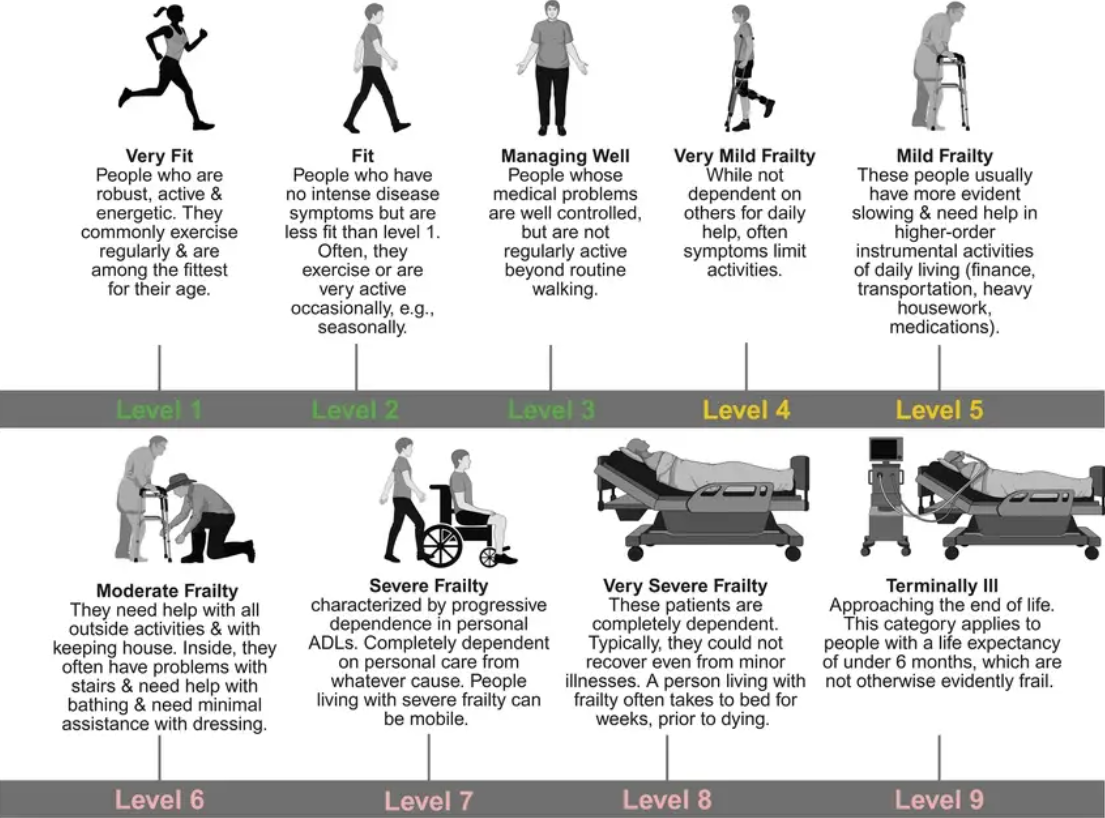
我们先来说说什么是衰老性虚弱。在临床医学中,衰老性虚弱是以“肌力下降、步速减慢、持续性疲劳、非预期性体重减轻、整体活动量萎缩”为特征的集合。把虚弱当成临床诊断标准,目的并不是制造更多病人,而是正视它对“健康寿命”的实质威胁。虚弱是进入失能期的前兆,是健康寿命与生存时间之间那段“活着但活得不好”的漫长前奏。
目前,全球65岁以上老年人中,估计有12%-24%处于虚弱状态,随着人口老龄化加剧,这一数字将持续攀升。
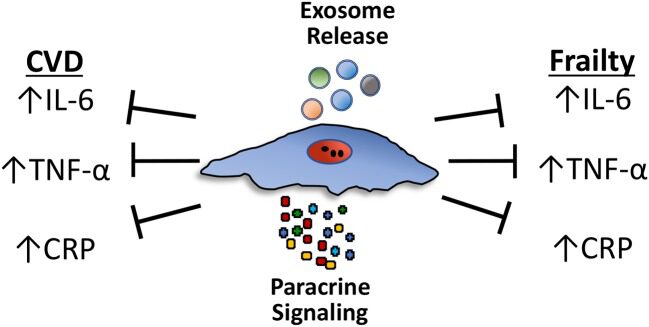
要理解虚弱的生物学根源,需要引入一个近年来越来越被接受的概念:炎症性衰老(inflammaging)。随着年龄增长,免疫系统的调控精度逐渐下降:一方面,针对外来病原体的防御能力减弱;另一方面,身体却持续向组织释放低水平的促炎信号,形成一种慢性的、低强度的系统性炎症状态。这种背景噪音式的炎症并无明显的急性症状,但它长期侵蚀肌肉、血管功能、神经系统效率与组织修复能力。衰老性虚弱,在很大程度上正是这种炎症积累到一定阈值后的系统性表现。
这次研究做了什么
今天要介绍的新研究是目前同类研究中设计最为严格的临床试验之一,采用随机、双盲、安慰剂对照设计,阶段为2b期,目标是在已确认安全性的前提下,进一步确定最优剂量并评估初步疗效。研究共纳入148名受试者,年龄介于70-85岁之间,可自主行走,但已被诊断为“轻度至中度衰老性虚弱”;受试者被随机分配到不同剂量的干细胞输注组或安慰剂组,接受单次静脉输注。
主要评估指标有两项:6分钟步行测试和患者自我报告的身体功能评分。前者是衡量体力状态的强指标:在受控条件下测定一个人6分钟内能走多远,其变化值在临床上具有公认意义。
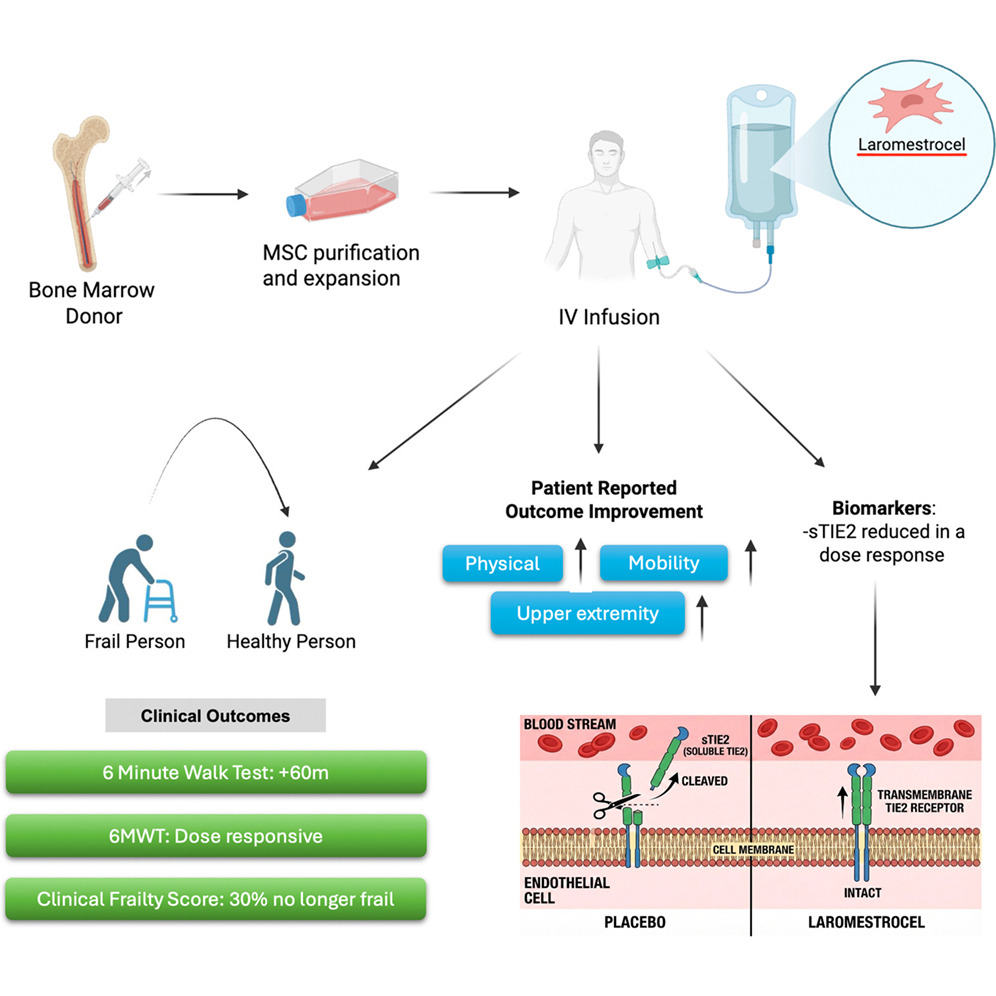
结果是明确的。在第9个月时,接受干细胞输注的受试者6分钟步行距离平均提升了63.4米。这一改善幅度超过了临床意义的最低门槛,且患者自我报告的功能评分与步行距离的提升呈正相关。
更值得关注的是,约30.8%的受试者在治疗后从“虚弱”状态转变为“非虚弱”状态。这提示该疗法并非只是延缓症状,而是有可能在功能层面上实现一定程度的逆转。
研究还识别出一个潜在的生物标志物:TIE2(酪氨酸激酶受体,与血管生成和血管稳定相关)。随着输注剂量增加,可溶性TIE2水平出现下降趋势,说明间充质干细胞可能通过改善血管微环境来间接恢复身体功能。这很重要,因为它暗示了一个机制路径:疗法产生效果,不只在于“补充”什么,还需要重建支持系统。
间充质干细胞为什么可能有用
听到“干细胞”,很多人脑子里出现的第一个画面,是科幻小说里的“再生”场景:受损的组织重新长出来,老化的器官焕然一新。这个印象并非完全错误,但放在间充质干细胞(MSCs)的语境下,需要做一些修正。
MSCs的身份:调度员+广播员
间充质干细胞是一类广泛存在于人体骨髓、脂肪组织和脐带等部位的多能间质细胞。按照国际细胞治疗学会(ISCT)的定义标准,MSCs须表达特定表面标志物(CD73、CD90、CD105),并具备在体外向骨、软骨、脂肪细胞分化的能力。这种分化潜能使它们在早期干细胞研究中主要被视为“组织修复的原料”。
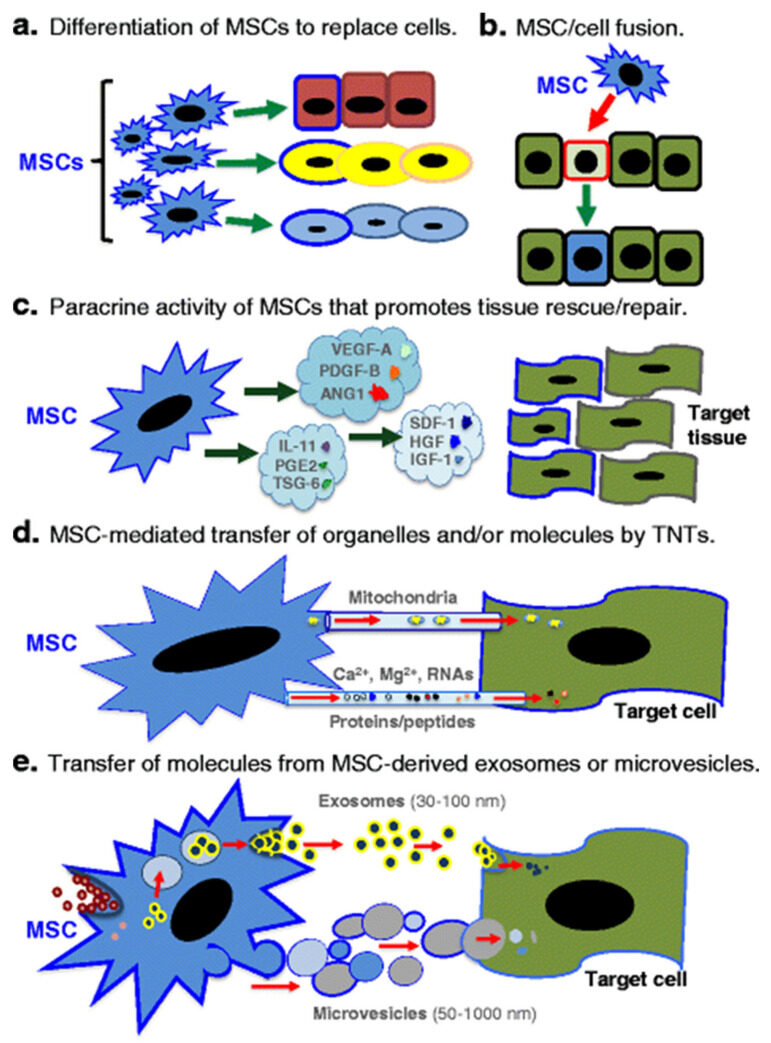
然而,大量后续研究逐渐澄清了一个关键事实:MSCs在体内发挥作用的核心机制并非直接分化为新组织,而是通过旁分泌方式调节周围的细胞环境。它们更像一个高效的调度员——输入到体内之后,通过释放信号分子来改变周围细胞的行为,而不是亲自上场干活。支持这一观点的重要证据来自一个现象:MSCs来源的细胞外囊泡(EVs),单独施用时能重现与MSCs细胞本身相近的治疗效果。
MSCs释放的是什么信号
MSCs通过旁分泌途径分泌的生物活性物质,涵盖三大类:细胞因子、生长因子,以及外泌体。
细胞因子层面,MSCs能够释放白细胞介素-10(IL-10)、转化生长因子-β(TGF-β)和前列腺素E2(PGE2)等抗炎介质,下调促炎因子(TNF-α、IL-1β和IL-6)的水平,并通过促进巨噬细胞从促炎的M1表型向抗炎修复的M2表型转化,重塑局部免疫微环境。
外泌体是近年来研究最为密集的方向。外泌体作为细胞间通讯的媒介,将信号传递给受体细胞并改变其生物学行为。这种传递方式具有高度的靶向效率,相较于简单地向细胞间隙注入细胞因子,外泌体能将特定信号更精准地送达目标细胞。
MSCs疗法在衰老相关疾病中的其他研究进展
对于间充质干细胞的研究并不是从衰老性虚弱开始的,它的整个临床开发历程反映了MSCs抗衰老潜力的多维度探索。
在阿尔茨海默病方向,一项2025年发表于 Nature Medicine 的2a期随机对照试验对轻度阿尔茨海默症患者进行了间充质干细胞的多次静脉输注,初步数据提示该疗法可能有助于减缓认知衰退和脑萎缩——尽管样本量有限,机制尚未完全厘清,但这是MSCs尝试跨越血脑屏障干预神经退行性疾病的重要临床信号。
在心血管领域,间充质干细胞来源的外泌体对心肌梗死后损伤的修复已有系统性研究积累,主要机制包括促进血管新生、抑制心肌细胞凋亡和减轻梗死后炎症反应。
在免疫与炎症疾病方向,间充质干细胞疗法已率先走到了临床应用的前沿。2024年12月,美国FDA批准了史上第一款间充质干细胞疗法的商业上市,适应症是儿科急性移植物抗宿主病(aGvHD),这是间充质干细胞在严重免疫失调状态下调节炎症能力的最直接临床验证。
还有骨关节炎方向。间充质干细胞注射治疗膝关节骨性关节炎的长期随访数据显示,单次治疗后3年内软骨缺损面积开始缩小,5年内无显著恶化。这一发现支持了一个观点:MSCs的主要作用机制不是直接再生软骨,而是通过重塑免疫微环境,为机体自身的修复过程创造条件。
回到衰老性虚弱:为什么MSCs对它有效
MSCs的这套调节机制,与衰老性虚弱的发病核心恰好形成了对应关系。前文提到,虚弱的生物学根基在于慢性低度炎症对全身系统的持续侵蚀。临床试验数据显示,静脉输注异体间充质干细胞可以改善虚弱患者的系统性健康生物标志物和免疫衰老相关指标。间充质干细胞的抗炎和免疫调节作用,本质上是在干扰这一炎症积累的过程——如果把虚弱比作一个长期低功率运转的嘈杂环境,间充质干细胞的介入更像是系统性降噪,而不是直接修补某个具体的零件。
这项研究对我们来说意味着什么
离更大规模的3期试验还有一段距离
这项新研究是迄今为止规模最大、设计最严格的针对衰老性虚弱的干细胞临床试验之一,但仍处于2b期阶段。2b期的核心任务是确认剂量范围、安全性,并提供足够的疗效信号以支撑后续的3期大规模试验。
但是证明它疗效的数据可信度高,更重要的是,它提供了一个可供验证的机制假说(TIE2/血管微环境路径)和一个可供放大的临床方案,为3期试验的设计奠定了基础。
现在能做什么?
虽然细胞疗法尚未触手可及,但这项研究所指向的生物学逻辑——延缓炎症积累、保持肌肉功能、维持血管微环境的健康——对应的是一些已有扎实证据的可行干预手段:
抗阻训练是其中证据最充分的一项。规律的抗阻运动可以延缓肌少症进程、降低系统性炎症标志物,并改善老年人的功能性体能表现。
充足的蛋白质摄入是肌肉合成代谢的物质基础。通常建议老年人每公斤体重1.2至1.6克/天。
控制慢性炎症相关的行为因素,也持续被老年医学研究证实与健康寿命呈正相关。比如,睡眠质量、压力管理和社交活跃度。
这项研究的背后,是整个衰老医学领域正在从单纯的症状管理,走向修复细胞和系统层面的损伤。我们对衰老的干预,正在变得更具体、更有依据,从而让健康老去不再只是运气。
参考资料: Ruiz JG, Oliva AA Jr, Ramdas KN, et al. Randomized phase 2b dose-escalation trial of stem cell therapy with laromestrocel for aging frailty. Cell Stem Cell. 2026;33(3):393-404.e4. doi: 10.1016/j.stem.2026.01.017. Rash BG et al. Allogeneic mesenchymal stem cell therapy with laromestrocel in mild Alzheimer's disease: a randomized controlled phase 2a trial. Nature Medicine. 2025;31:1257–1266. Brody M et al. Results and insights from a phase I clinical trial of Lomecel-B for Alzheimer's disease. Alzheimers Dement. 2023;19:261–273. Tompkins BA et al. Allogeneic mesenchymal stem cells ameliorate aging frailty: a phase II randomized, double-blind, placebo-controlled clinical trial. J Gerontol A Biol Sci Med Sci. 2017;72:1513–1522. Garay RP. Recent clinical trials with stem cells to slow or reverse normal aging processes. Front Aging. 2023. DOI: 10.3389/fragi.2023.1148926 Han Y et al. The secretion profile of mesenchymal stem cells and potential applications in treating human diseases. Signal Transduct Target Ther. 2022;7:92. López-Otín C, Kroemer G, Serrano M. The hallmarks of aging: 2023. Cell. 2023;186(8):2431–2468. Al-Azab M et al. Aging of mesenchymal stem cell: machinery, markers, and strategies of fighting. Cell Mol Biol Lett. 2022;27:69. Dominici M et al. Minimal criteria for defining multipotent mesenchymal stromal cells. Cytotherapy. 2006;8(4):315–317. Deng S et al. Exosomes from adipose-derived mesenchymal stem cells ameliorate cardiac damage after myocardial infarction. Int J Biochem Cell Biol. 2019;114:105564.
