我们为什么会变老?我们究竟有多老?我们该如何延缓衰老?衰老领域的研究,始终围绕这几大经典问题展开。 2013年,西班牙科学家卡洛斯·洛佩斯-奥廷(Carlos López-Otín)提出衰老的九大标志,为精准干预衰老提供了明确靶点,十几年来,衰老研究领域的飞速发展,衰老相关的认知不断进阶迭代,研究手段也日益精细化。 近期,中科院动物所刘光慧研究员带领的中国衰老标志物研究联合体(Aging Biomarker Consortium, ABC),在《Nature Reviews Molecular Cell Biology》上发表了一篇具有里程碑意义的综述文章。文章系统梳理了衰老过程中,人类和非人灵长类动物在细胞、组织和个体层面的关键生物标志物[1],为人类衰老研究锁定了更加精准的方向。 衰老是一个渐进的过程,受到物种寿命、基因组稳定性以及细胞修复能力等多重因素的影响。 在寿命较短的动物(如线虫、果蝇、大鼠、小鼠等)中,评估衰老进程及其终点,以及长寿干预对寿命的影响相对简单。然而,这些模型并不适用于寿命较长的灵长类动物,尤其是人类。 人类作为长寿物种,其衰老机制更加复杂,难以通过简化的动物模型复制和研究。 非人灵长类动物在衰老研究中具有天然的优势。它们与人类在生理结构、基因组以及免疫系统等方面具有高度的相似性。因此,能在与人类相似的时间尺度内观察衰老过程,从而提升了其在衰老研究中的实用性和相关性。 毫无疑问,非人灵长类动物是研究衰老的最理想模型。但是,非人灵长类动物的高成本仍是一个现实问题,许多实验室面临投入与产出的权衡。 寿命并不是评估衰老或相关疾病干预效果的最佳指标,因为许多治疗方法能延长健康寿命,但对最大寿命影响有限。因此,研究衰老生物标志物尤为重要。这些标志物能够量化细胞损伤和生理衰退,作为生物年龄的衡量标准,并帮助评估衰老进程、年龄相关疾病以及干预效果。 首先,研究人员系统总结了细胞层面的十大衰老标志物:细胞周期停滞、基因组完整性丧失、端粒缩短、表观遗传不稳定性、核结构改变、线粒体功能障碍、溶酶体功能障碍、蛋白质稳态失衡、代谢失调以及衰老相关分泌表型 (SASP)。 在组织层面,跨学科的研究证据系统性地评估了各器官的结构性和功能性衰老标志。包括皮肤、脑、脊髓、肺、肝脏、脂肪、肌肉、骨骼、肾脏、免疫系统、心血管系统和生殖系统等,均呈现出特有的衰老特征。 例如,大脑衰老表现为脑萎缩与认知功能下降;血管衰老则表现为血管硬化和钙化;肝脏衰老则导致代谢功能下降及脂肪堆积等等。 在个体层面,研究者们正在开发整合性评估工具,如衰老时钟以及临床常规标志物的应用前景。其中,虚弱指数作为一个由34个健康变量构建的综合指标,涵盖心血管、呼吸、认知和功能缺陷,已被证明能有效指示人类的生物年龄。 此外,临床血液评估也显示,血红蛋白浓度、红细胞计数和血细胞比容值在老年人群体中普遍下降,表明这些生物标志物在衰老研究中的潜力。 随着衰老机制的逐步揭示,科学家们在探索如何干预衰老的过程中取得了显著进展。近年来,一些抗衰老干预方法在灵长类动物中显示出了积极的效果,带来了对人类抗衰老的希望。 这类药物能特异性清除衰老细胞,改善动物的认知能力和运动能力。 例如,“达沙替尼+槲皮素”组合就在食蟹猴中表现出显著效果,不仅减轻了衰老相关表型,还改善了整体健康状况[3]。 人类临床研究表明,达沙替尼和槲皮素的联合治疗能减少脂肪组织中的衰老细胞,提升脂肪前体细胞的增殖能力,并改善皮肤组织的健康。此外,还能改善阿尔茨海默症患者的认知功能[4,5]。 调节代谢药物已被证明有延缓衰老的潜力。 在食蟹猴中,牛磺酸补充能够减少脂肪堆积、增加骨密度,并降低氧化应激标志物[6]。二甲双胍则表现出抗衰老保护作用,改善认知表现并通过衰老时钟评估显示出衰老逆转效果[7]。 适度的运动能够降低体内炎症水平,提升细胞的修复能力,从而延缓衰老[8]。 干细胞具有强大的自我修复能力,移植年轻干细胞能够促进全身性衰老的延缓,并增强免疫功能。 例如,向食蟹猴体内移植抗衰老的干细胞,能够促进系统性年轻化,降低衰老标志物IL-1β和γ-H2AX的水平[9]。 这些抗衰老策略在灵长类动物模型中的验证,也给人类抗衰老干预带来了新的希望。 那么我们如何判断自己有多老呢?有的人60岁看起来像40岁,而有的人40岁却像60岁,单纯依靠年龄显然无法准确反映生理状态。 自此,除了经典的“表观遗传时钟”,研究人员还相继开发了多种新型生物时钟,从转录组、蛋白质组、代谢组到免疫状态,甚至面部形态,都能为我们提供衰老的多维度评估。 这些时钟为全面了解生理年龄与健康风险提供了新的视角。 但这些模型大多基于西方人群数据,是否适用于中国人?答案可能是否定的。 考虑到衰老受多种因素影响,而现有时钟大多依赖西方人群的研究数据,中国衰老标志物研究联合体(ABC)在2025年9月启动了“X-Age”(耄耋计划)项目,旨在为中国人群打造一个科学、可靠的衰老评估系统,制定更适合中国人的健康衰老策略。 这是中国首个系统性、大规模、多模态的衰老研究平台。X-Age将通过结合多组学数据(如基因组、代谢组等)与AI技术,致力于为中国人群构建一个多维度的衰老评估系统,克服现有衰老时钟的局限性,开发一个更为精准和个性化的衰老时钟。 这足可见我国科学家为推动我国衰老干预策略研究、精准医学以及健康管理发展的决心。 随着全球衰老生物标志物框架的逐步建立,以及中国在衰老干预领域的创新突破,研究成果也逐渐在国际上崭露头角,彰显了中国在这一领域的学术权威。 然而,衰老的本质是个体化、高度异质的过程,尚未有某种单一标志物能适用于所有人。未来,我们仍需要借助人工智能、多组学数据以及大型队列研究,构建更精确、更具预测性的衰老评估系统。 如今,“细胞衰老网络(SenNet)”等国际计划正推动利用计算组学深入解析细胞与组织衰老机制[10],也预示着精准抗衰老的新时代正在到来。
为什么是灵长类?人类衰老研究的理想模型

衰老的标志:从细胞、组织到个体的全方位演变
细胞层面:衰老的基础标志
组织层面:器官衰老的特异性表现
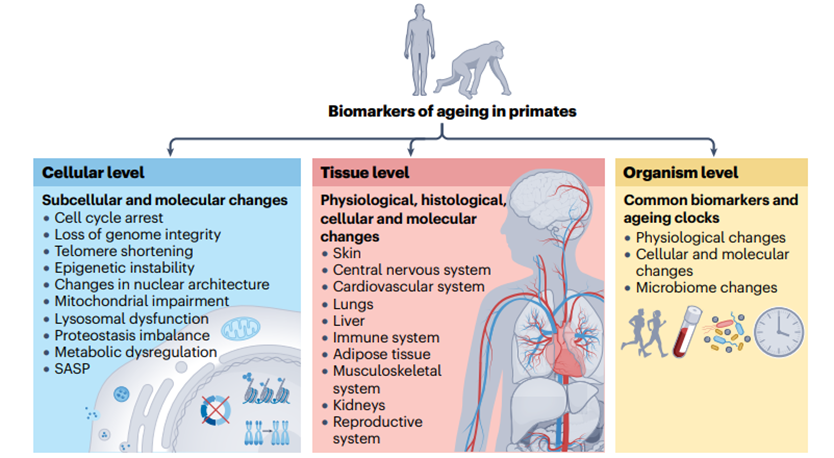
个体层面:个体衰老的整合性评估
抗衰老干预:从猴子到人类的希望
Senolytics(衰老细胞清除剂):
代谢调节干预:
运动:
干细胞疗法:
“衰老时钟”:不止是DNA甲基化

耄耋计划:构建中国人自己的衰老时钟
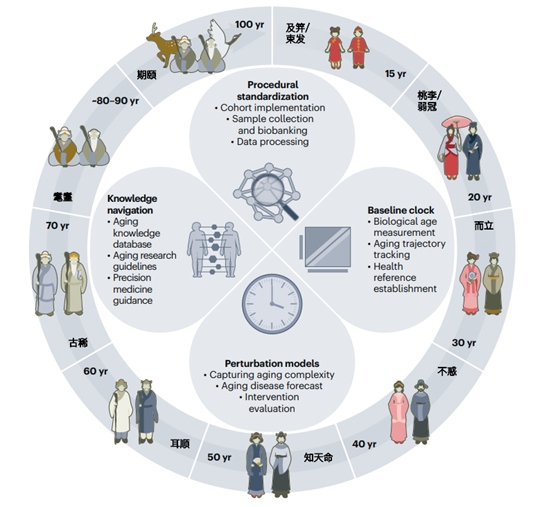
精准抗衰老时代即将到来
Cover designed by freepik.
[1]Wu, Z., Qu, J., Zhang, W. & Liu, G.-H. Biomarkers of ageing of humans and non-human primates. Nature Reviews Molecular Cell Biology (2025) doi:10.1038/s41580-025-00883-8. [2]Li, J. et al. The X-Age Project to construct a Chinese aging clock. Nature Aging (2025) doi:10.1038/s43587-025-00935-w. Online ahead of print. [3]Ruggiero, A. D. et al. Long-term dasatinib plus quercetin efects on aging outcomes and inflammation in nonhuman primates: implications for senolytic clinical trial design. Geroscience 45, 2785–2803 (2023). [4]Hickson, L. J. et al. Senolytics decrease senescent cells in humans: preliminary report from a clinical trial of dasatinib plus quercetin in individuals with diabetic kidney disease. eBioMedicine 47, 446–456 (2019). [5]Millar, C. L. et al. A pilot study of senolytics to improve cognition and mobility in older adults at risk for Alzheimer’s disease. eBioMedicine 113, 105612 (2025). [6]Singh, P. et al. Taurine deficiency as a driver of aging. Science 380, eabn9257 (2023). [7]Yang, Y. et al. Metformin decelerates aging clock in male monkeys. Cell 187, 6358–6378.e29(2024). [8]Geng, L. et al. Systematic profiling reveals betaine as an exercise mimetic for geroprotection. Cell. https://doi.org/10.1016/j.cell.2025.06.001 (2025). [9]Lei, J. et al. Senescence-resistant human mesenchymal progenitor cells counter aging in primates. Cell. https://doi.org/10.1016/j.cell.2025.05.021 (2025). [10]Li, S. et al. Advancing biological understanding of cellular senescence with computational multiomics. Nature Genetics (2025) doi:10.1038/s41588-025-02314-y.
